حرارة التكوين Heat of formation
- ينتج عن تكوين المركب من عناصره الأولية انطلاق او امتصاص قدر من الطاقة يساوي المحتوى الحراري له يعرف بحرارة التكوين ΔHF
- حرارة التكوين هي كمية الحرارة المنطلقة أو الممتصة عند تكوين المركب من عناصره الأولية
- وإذا كانت العناصر المكونة للمركب في حالتها القياسية والتى تمثل أكثر حالات المادة استقراراُ في الظروف القياسية ، فأن التغير الحرارى المصاحب لتكوين المركب يعرف بحرارة التكوين القياسية ΔHFo
حرارة التكوين القياسية Standard Heat of formation
- هى كمية الحرارة المنطلقة أو الممتصة عتد تكوين مول واحد من المركب من عناصره الأولية بشرط أن تكون في حالتها القياسية.
- وحدة قياس حرارة التكوين: kJ/mol
- ولقد اتفق أن قیم لجمیع العناصر في حالتھا القیاسیة تساوي صفراً
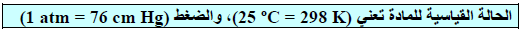
أمتلة توضيحية
(1) الأكسجين یوجد على ثلاثة أشكال :
الأكسجين الذري (O) ، والأكسجين الجزيئي (O2) ، الأوزون (O3)
ويعتبر الأكسجين (O2) الأكثر استقراراً عند (298K) وضغط جوي واحد (1 atm) وبالتالي فإن:
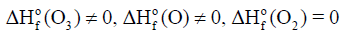
(2) الكربون یوجد على شكلین:
جرافيت (graphite) وألماس (diamond) ویعتبر الجرافیت الأكثر استقراراً عند (298 K) وضغط جوي واحد ، وهذا يعني:
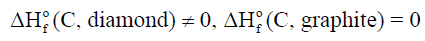
شروط كتابة معادلة التكوين
(1) المادة الناتجة ھي فقط مول من المادة المراد إیجاد حرارة التكوین لھا.
(2) المواد المتفاعلة ھي العناصر المكونة للمادة المراد إیجاد حرارة التكوین لھا. بشرط أن تكون ھذه العناصر في الحالة القیاسیة.
فمثلاً لا یمكن استخدام التفاعل التالي لحساب حرارة التكوین لـــ CO
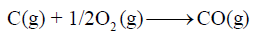
وذلك لأن الكربون في حالته الطبیعیة یكون في حالة صلبة ولیست غازیة.
أمثلة توضيحية
(1) حرارة التكوین لكلورید الھیدروجین HCl
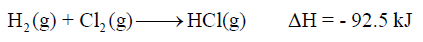
(2) حرارة التكوین للماء H2O
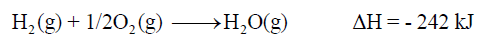
(3) حرارة التكوین لأكسید الكربون CO
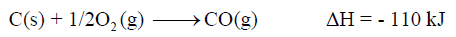
حساب حرارة التكوين القياسية
مثال (1): لديك التفاعل التالي:
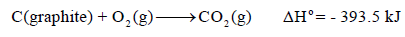
وفيه حرارة التفاعل القياسية ΔHo (التغير في الإنثالبي القياسي) یساوي مجموع حرارات التكوین القیاسیة لجمیع المواد الناتجة مطروحاً منه مجموع حرارات التكوین القیاسیة لجمیع المواد المتفاعلة، أي:
حيث:
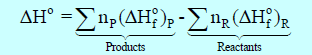
P تعني Products أي النواتج
R تعني Reactants أي المتفاعلات .
ΔHo : حرارة التفاعل
np= عدد المولات لأى مادة ناتجة
nR = عدد مولات لأى مادة متفاعلة .
ΔHFo)p) = حرارة التكوین لمول واحد من المادة الناتجة
ΔHFo)R) = حرارة التكوین لمول واحد من المادة المتفاعلة
وبالتالي فإنه للتفاعل:
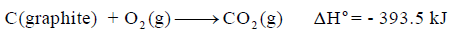
یمكن حساب حرارة التفاعل أو حرارة التكوین لأي مادة متفاعلة كما یلي :
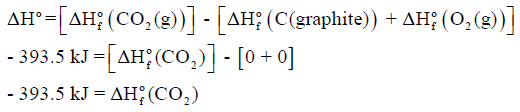
وھذا یعني أن حرارة التفاعل القیاسیة ΔHο تساوي حرارة التكوین القیاسیة للمركب (CO2(g