أولاً: الخواص الفيزيائية للفلزات القلوية Alkali Metals
- تضم الفلزات القلوية: الليثيوم - الصوديوم - البوتاسيوم - الروبيدوم - السيزيوم - الفرنسيوم.
- للفلزات القلوية مظهر فضي لامع.
- تكون الفلزات القلوية الصلبة لينة لدرجة يمكن قطعها بالسكين.
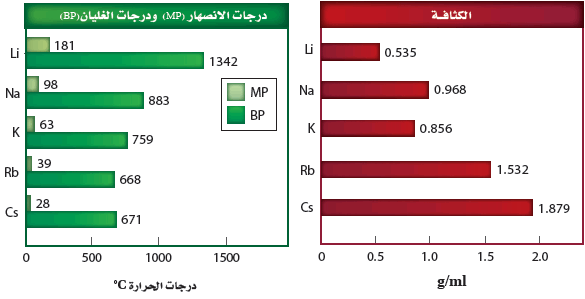
- لمعظم الفلزات القلوية كثافة منخفضة مقارنة بالعناصر الصلبة التابعة للمجموعات الأخرى.
فعلى سبيل المثال تكون كثافة كل من الصوديوم والليثيوم والبوتاسيوم أقل من كثافة الماء.
- للفلزات القوية درجات انصهار منخفضة مقارنة بالفلزات الأخرى، ومنها الفضة والذهب.
ثانياً: الخواص الذرية للفلزات القلوية
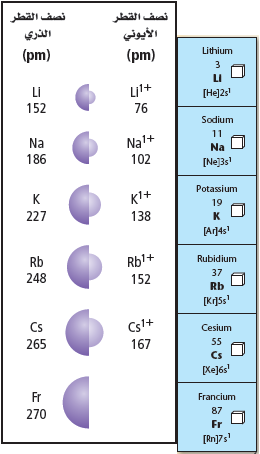
- لكل عنصر من عناصر المجموعة الأولي إلكترون تكافؤ واحد وتوزيع إلكتروني ينتهي بـ nS1
- تفقد عناصر المجموعة الأولى إلكترون التكافؤ الخاص بها لتكون أيونًا ذا شحنة موجبة (1+)
- تزداد أنصاف أقطار الذرات وأنصاف أقطار الأيونات كلما انتقلنا في المجموعة الأولي من أعلى إلى أسفل.
- تقل الكهروسالبية كلما انتقلنا في المجموعة الأولى من أعلى إلى أسفل.
- لا توجد الفلزات القلوية في الطبيعة بشكل حر؛ لأنها نشطة جدًّا.
- لكل عنصر من عناصر الفلزات القلوية نظير واحد مشع على الأقل.
- بسبب ندرة عنصر الفرانسيوم، ولأنه يضمحل بسرعة كبيرة جدًّا فإن خواصه غير معروفة إلى الآن
- فيمايلى قيم السالبية الكهربية وطاقة التأين الأولى للفلزات القلوية:
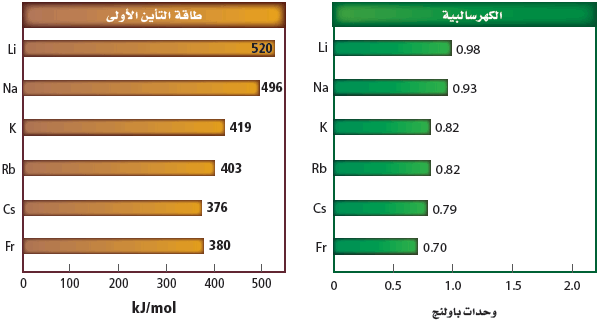
- فيما يلي قيم التوزيع الألكتروني لعناصر المجموعة الأولى قيم أنصاف الأقطار للذرة والأيون الموجب:
ثالثاً: الأختبارات التحليلية
يمكن تعريف الفلزات القلوية من خلال اختبارات اللهب؛ فالليثيوم ينتج لهبًا أحمر والصوديوم ينتج لهباً برتقالياً ، بينما ينتج كل من البوتاسيوم والروبيديوم والسيزيوم لهبًا بنفسجيًّا.
