قوة الاحماض الاكسجينية
- يتم تمثيل الحمض الاكسجينى [MOn(OH)m] حيث M هى ذرة العنصر
- تعتمد قوة الاحماض الاكسجينية على عدد ذرات الأكسجين الغير مرتبطة بالهيدروجين
- الحمض الأقوى هو الذى يحتوى على عدد أكبر من ذرات الاكسجين (On) الغير مرتبطة بالهيدروجين
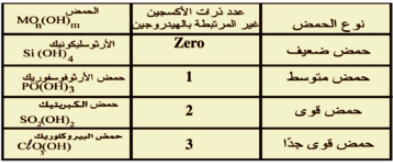
(أ) n = 0 يكون الحمض ضعيفاً جداً مثل :
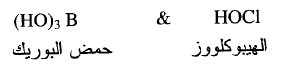
(ب) n = 1 يكون الحمض ضعيفاً مثل :
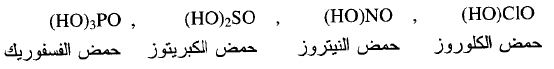
(جـ) n = 2 يكون الحمض قوياً مثل :

(د) n = 3 يكون الحمض قوياً جداً مثل :

حل السؤال: عناصر مختلفة ترتيب أنصاف الأقطار لها: X > Z > Y وتكون هذه العناصرالأحماض H2ZO2, H4YO4, HXO رتب الأحماض حسب قوتها؟
الحل:
- يتم تمثيل الحمض الاكسجينى [MOn(OH)m]حيث M هى ذرة العنصر فيكون الأحماض الموجودة فى المسألة كالتالي:
H2ZO2, H4YO4, HXO
Z(OH)2 ,Y(OH)4 , X(OH)1
- تعتمد قوة الاحماض الاكسجينية على عدد ذرات الأكسجين الغير مرتبطة بالهيدروجين ولكن هنا لا توجد ذرات أكسجين غير مرتبطة بذرة العنصر لذلك فكلها أحماض ضعيفة حيث n = 0
- تزداد الخاصية الحامضية بزيادة العدد الذرى الذي يؤدى إلى زيادة نصف قطر ذرة العنصر بذلك تقل قوة جذب النواة لأيون الهيدروجين فيسهل تأينه.
- وكلما أصبح الحمض سهل التأين (سهولة خروج أيونات الهيدروجين) كلما كان الحمض أقوي
فيكون:
X > Z > Y
X(OH)1 > Z(OH)2 > Y(OH)4