أولاً/ إستنتاج العلاقة بين المولارية بالكثافة والنسبة المئوية الوزنية
- المولارية هي عدد المولات من المذاب فى لتر من المحلول ويرمز لها بالرمز (M)
- الصيغة الرياضية لحساب المولارية تعطى من القانون التالي:
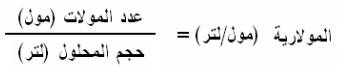
- يحسب عدد المولات من القانون التالي:
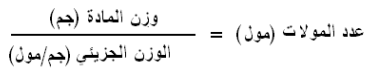
وبالتعويض فى القانون الأول عن عدد المولات نحصل على:

وبما أن الكثافة = وزن المحلول / حجم المحلول فأنه حجم المحلول يعطى من العلاقة التالية:
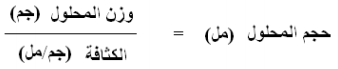
وعند تحويل الحجم إلى لتر وذلك بقسمة الطرفين على 1000 فإن العلاقة السابقة تصبح:

يمكن التعويض عن حجم المحلول فى قانون المولارية ويكون:

ويمكن كتابته كالتالي:

وبترتيب الحدود على الكسر فأن:

وحيث أن النسبة المئوية الوزنية تعطى كالتالي:
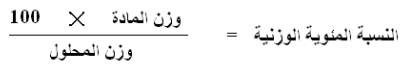
وبالتعويض فى القانون أعلاه نحصل على القانون التالي:

ثانياً / استنتاج العلاقة بين العيارية والنسبة المئوية الوزنية والكثافة
من قانون العلاقة بين المولارية والعيارية
العيارية = المولارية * التكافؤ
نعوض عن ذلك فى القانون الملون بالأصفر الخاص بالمولارية ثم نعوض عن:
الوزن المكافئ = الوزن الجزيئي / التكافؤ
نحصل على القانون التالي:
