تفاعلات الأكسدة والاختزال
Oxidation - Reduction Reactions
- يمكن التمييز بين تفاعلات الأكسدة والاختزال وغيرها ، وذلك من خلال تغير عدد الأكسدة للعنصر في المواد المتفاعلة عنه في المواد الناتجة.
- ويمكن توضيح ذلك من خلال المثال التالي:
مثال (1): صنف تفاعلات الاكسدة والاختزال عن غيرها لما يلي:
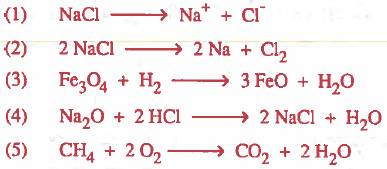
الحل:
نكتب اعداد الأكسدة لكل عنصر في البداية:
(1)
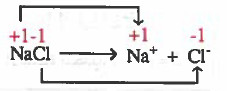
يتضح أن العناصر لم تتغير أعداد أكسدتها ، وهذا يعني أنه لم يحدث أكسدة أو اختزال.
(2)
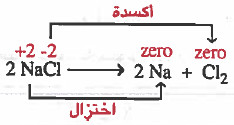
لاحظ أن أعداد الأكسدة تغيرت لبعض الذرات وهذا يعني أن التفاعل تفاعل أكسدة واختزال.
(3)
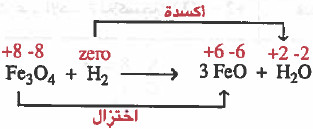
لاحظ أن أعداد الأكسدة تغيرت لبعض الذرات وهذا يعني أن التفاعل تفاعل أكسدة واختزال.
(4)
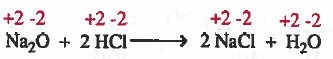
يتضح أن العناصر لم تتغير أعداد اكسدتها ، وهذا يعني أنه لم يحدث أكسدة او اختزال.
(5)
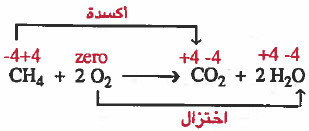
لاحظ أن أعداد الأكسدة تغيرت لبعض الذرات وهذا يعني أن التفاعل تفاعل أكسدة واختزال.
كيفية كتابة نصفي التفاعل لمعادلات الأكسدة والاختزال
- يمكننا كتابة نصفي التفاعل لأي معادلة كما يلي:
(1) التعرف على اعداد الأكسدة لكل عنصر في المعادلة.
(2) فصل العنصر الذي حصل له أكسدة وناتجه في معادلة ، مع كتابة عدد الإلكترونات المفقودة في الجهة اليمنى (النواتج).
(3) فصل العنصر الذي حصل له اختزال وناتجه في معاملة ، مع كتابة عدد الإلكترونات المكتسبة في الجهة اليسرى (المتفاعلات).
(4) وزن الإلكترونات في نصفي المعادلة وذلك بضرب المعادلتين في عدد بحيث تتساوى أعداد الإلكترونات .
مثال (2): اكتب نصفي تفاعل الأكسدة والاختزال للتفاعل التالي :
A1 + 2 H+ → Al3+ + H2
الحل:
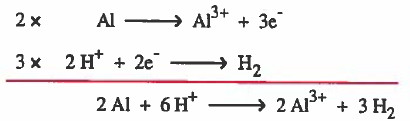
ملاحظة:
يمكن وزن معادلات الاكسدة والاختزال بطرقتين:
(۱) طريقة الايون - إلكترون ( طريقة نصف التفاعل).
(۲) طريقة اعداد الأكسدة.