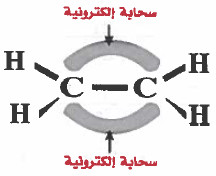
الروابط المتعددة Multiple Bonds
- تتكون الرابطة الثنائية أو الثلاثية عندما يقتسم زوجان أو ثلاثة أزواج إلكترونية بين ذرتين على التوالي.
الرابطة الثنائية Doubel Bond
- ومن أشهر الأمثلة على الرابطة الثنائية جزيء الإيثلين C2H4.
- وسوف يتم توضيح كيفية تكون الروابط في جزيء C2H4 كما يلي:
(1) نكتب التركيب الإلكتروني لذرة الكربون في الحالة المستقرة (المنفردة):
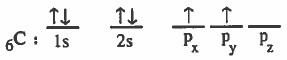
(2) التركيب الإلكتروني لذرة الكربون في الحالة المثارة:
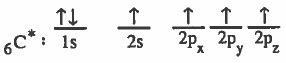
(3) يحدث دمج (تهجين) بين المجال (2S) ومجالين من (2p) وهما ( 2px, 2py ) لينتج ثلاثة مجالات مهجنة متساوية في الشكل والطاقة كل منها يسمى sp2 ويبقى المجال 2pz دون تهجين ويكون عمودياً على المستوى الذي يمر بالمجالات sp2
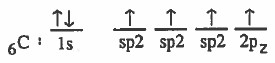
وبعد ذلك يحدث نوعان من التداخل وهما :
(1) تداخل رأسي والروابط فيه من نوع سيجما (σ) كما يلي:
- التداخل بين المجالين ( sp2 - sp2 ) وينتج عنه رابطة بين (C-C).
- التداخل بين المجالين ( 1s - sp2) وينتج عنه رابطة بين ( C-H ).
(2) تداخل جانبي والروابط فيه من نوع باي (π) كما في التداخل بين المجالين ( 2pz - 2pz)
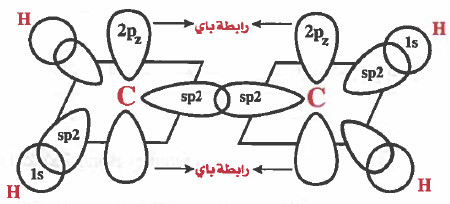
ملاحظة:
نتيجة لوجود تداخل جانبي بين المجالين ( 2p ) سوف تتكون سحابة إلكترونية من الأعلى ومن الأسفل كما في الرسم التالي: