ثابت سرعة التفاعل Reaction rate constant
- ثابت سرعة التفاعل هو الثابت الموجـود في قانون سرعة التفاعل ، وهو ثابت عند نفس درجـة الحـرارة وكل تفاعل له ثابت مميز له.
- وحدة ثابت سرعة التفاعل تعتمد على رتبة التفاعل ، أي أنها تختلف من تفاعل من الرتبة الأولى إلى تفاعل من الرتبة الثانية وهكذا.
- العوامل التي تؤثر على ثابت سرعة التفاعل هي كما يلي:
(۱) طبيعة المواد المتفاعلة
(۲) درجة الحرارة
- التفاعلات السريعة لها ثابت سرعة كبير القيمة ، والتفاعلات البطيئة لها ثابت سرعة صغير القيمة .
- تزداد قيمة ثابت سرعة التفاعل بزيادة درجة الحرارة .
استنتاج وحدات ثابت سرعة التفاعل
وحدة ثابت سرعة التفاعل تعتمد على رتبة التفاعل ، أي أنها تختلف من تفاعل من الرتبة الأولى إلى تفاعل من الرتبة الثانية وهكذا.
(1) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة صفر
نفرض تفاعل من الرتبة صفر:
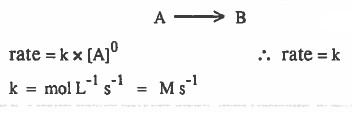
(2) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة الأولى
نفرض تفاعل من الرتبة الأولى :
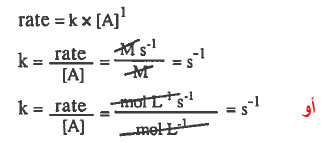
(3) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة الثانية
نفرض تفاعل من الرتبة الثانية:
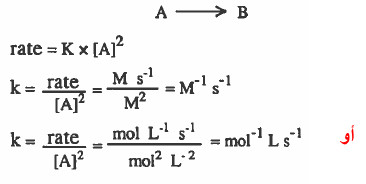
(4) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة الثالثة
نفرض تفاعل من الرتبة الثالثة:
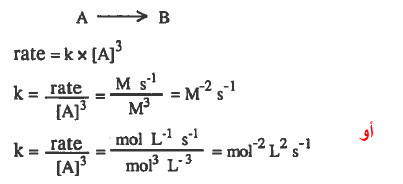
(5) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة الرابعة
نفرض تفاعل من الرتبة الرابعة:
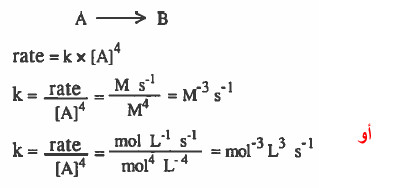
(6) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة 1/2
نفرض تفاعل من الرتبة 1/2
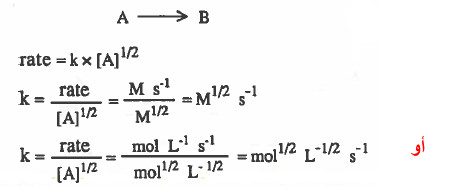
(7) استنتاج وحدة ثابت سرعة التفاعل لتفاعل من الرتبة 3/2
نفرض تفاعل من الرتبة 3/2:
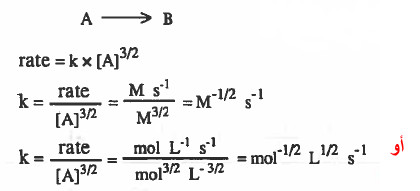
ملخص وحدات ثابت سرعة التفاعل
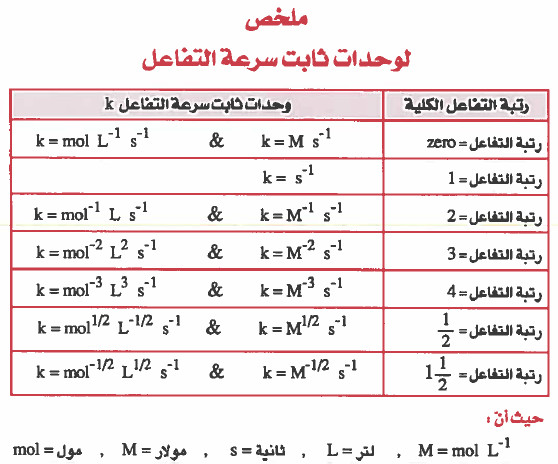
مسائل محلولة لحساب وحدات قياس ثابت التفاعل
مثال ( 1): مـا وحـدات ثابت سرعة التفاعل للتـفـاعـلات الـتـالـيـة إذا كـان قـوانـين سرعاتها كما يلي علماً بأن سرعاتها بوحدة : mol / L . s
(1) rate = k [A]0
rate = k [A]0 [B] (2)
(3) rate = k [A] [B]2
الحل:
(1) رتبة التفاعل من الدرجة صفر.
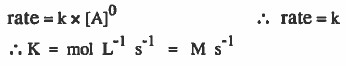
(2) رتبة التفاعل من الدرجة الأولى.
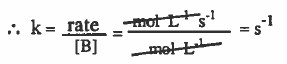
(3) رتبة التفاعل من الدرجة الثالثة.
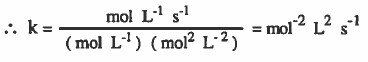
مثال (2): حسب التفاعل التالي:
A → B
فإذا كان تركيز المادة (A) يساوي 0.2mol / L وسرعة التفاعل 0.04mol / L . s فـاحـسـب قيمة ثابت سرعة التفاعل ووحدته عندما يكون التفاعل:
(1) من الرتبة صفر
(2) من الرتبة الأولى
(3) من الرتبة الثانية
(4) من الرتبة الثالثة
الحل:
