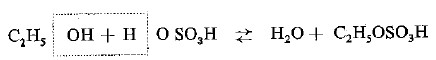الأيثرات
- يمكن النظر إلى الايثرات كبلا ماء الكحولات (انهيدريدات الكحولات).
- يمكن تحضيرها بنزع الماء من جزيئتين من الكحول باستعمال مادة نازعة للماء كحمض الكبريتيك المركز H2SO4.
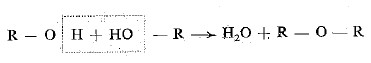
تحضير الأيثر الإيثيلي فى المعمل
- ضع في أنبوب اختبار قطرتين من الكحول الإيثيلي وقطرتين من حمض الكبريتيك المركز.
- سخن تسخيناً جذرياً على لهب حتى بداية اسمرار المحاول.
- يعزى ظهور الأسمرار إلى حدوث تفاعلات ثانوية نتيجة للتفحم الجزئي للكحول بفعل حمض الكبريتيك المركز.
- يمكن إثبات تكون الإيثر الإيثيلي من رائحته المميزة.
- أضف إلى المزيج الساخن قطرتين أخريين من الكحول الإيثيلي ، فيتكون دون تسخين إضافي كمية أخرى من الأيثر الإيثيلي الذي تصبح رائحته أكثر وضوحاً . قارن رائحته مع الإيثر الإيثيلي الجاهز.
مراحل التفاعل
- يجري التفاعل على مرحلتين.
- فعند بداية التسخين بتفاعل الكحول تدريجياً مع حمض الكبريتيك مكوناً كبريتات الإيثيل الحامضية:
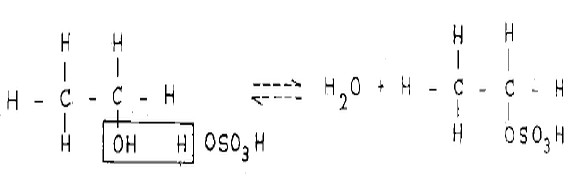
- فإذا كانت كمية حمض الكبريتيك المستعملة كبيرة وكمية الكحول قليلة فإن استمرار تسخين كبريتات الأيثيل الحامضية يعطي الايثيلين وحمض الكبريتيك الذي يتولد في هذه الحالة من الجزيئة نفسها نتيجة لانفصال مجموعة الكبريتات الحامضية مع ذرة الهيدروجين المرتبطة بذرة الكربون المجاورة .
- على العكس فإنه عندما تكون كمية الكحول أكبر نسبياً من كمية حمض الكبريتيك فإن الناتج يكون أثيراً.
- من الواضح أن حمض الكبريتيك يتولد في هذه الحالة من انفصال ذرة الهيدروجين الموجودة في جزيئة الكحول مع محموعة الكبريتات الحامضية الموجودة في جزيئة كبريتات الايثيل الحامضية.
معادلات تحضير الإيثر الإيثيلي
- وفيما يلي المعادلات الموضحة لذلك:
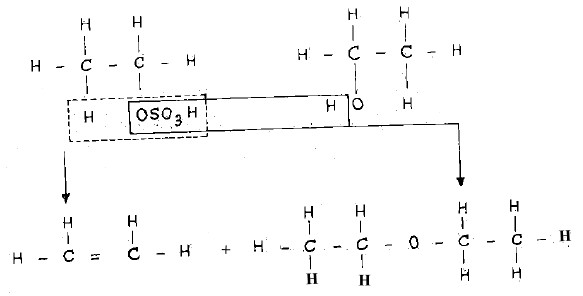
- هكذا إن حمض الكبريتيك المتولد يدخل ثانية في التفاعل مع كمية أخرى من الكحول.
- يتوقف التفاعل عندما تزداد كمية الماء فإن التفاعل يتكرر فيتحقق التوازن بين سرعة تكون كبريتات الأيثيل الحامضية وبين سرعة تميؤها.