حرارة التكوين Heat of Formation
- تعرف حرارة التكوين ΔHFo بأنھا حرارة التفاعل أو التغیر في الإنثالبي (المنطلقة أو الممتصة) عندما یتكون مول واحد من مادة ما من عناصرها الأولية وھي في حالتھا القیاسیة.
- وحدة قياس حرارة التكوين: kJ/mol
- ولقد اتفق أن قیم لجمیع العناصر في حالتھا القیاسیة تساوي صفراً
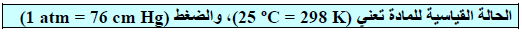
أمتلة توضيحية
(1) الأكسجين یوجد على ثلاثة أشكال :
الأكسجين الذري (O) ، والأكسجين الجزيئي (O2) ، الأوزون (O3)
ويعتبر الأكسجين (O2) الأكثر استقراراً عند (298K) وضغط جوي واحد ( 1atm) وبالتالي فإن:
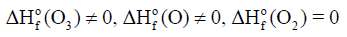
(2) الكربون یوجد على شكلین:
جرافيت (graphite) وألماس (diamond) ویعتبر الجرافیت الأكثر استقراراً عند (298K) وضغط جوي واحد ، وهذا يعني:
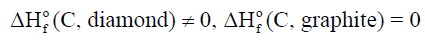
حرارة تكوين الهيليوم
- مما سبق نستنتج أن حرارة تكوين الهليوم القياسية = صفر عند الظروف القياسية كما ذكر أعلاه.
ΔHf°(He) = 0 kJ/mol
- أما بالنسبة لحرارة تكوين +He يمكنك الاطلاع على الرابط التالي:
ُُEnthalpy of formation of He Cation
- ويمكنك قراءة موضوع كامل عن حرارة التكوين من خلال موقع تعرف على علم الكيمياء
حرارة التكوين Heat of Formation + مسائل محلولة