(1) تفاعل ايونات الحديدوز مع كبريتيد الهيدروجين
تتفاعل مركبات الحديدوز مع كبريتيد الهيدروجين ينتج عنه تكون راسب بنى من كبريتيد الحديدوز.طبقاً للمعادلة:
Fe+2 + H2S → FeS↓+ H2
(2) إجراء التفاعل السابق فى حالة وجود حمض الهيدروكلوريك المركز
يتفاعل كبريتيد الحديدوز الناتج مع حمض الهيدروكلوريك المركز وينتج كلوريد الحديدوز (عديم اللون) وغاز كبريتيد الهيدروجين (له رائة البيض الفاسد) وفقاُ للمعادلة:
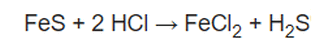
حيث يعتبر حمض الهيدروكلوريك المركز كاشف للشق الحامضى (ايون الكبريتيدات).
ولكن ماذا إذا كان الملح المطلوب الكشف عنه هو كلوريد الحديدوز
تتفاعل كلوريد الحديدوز مع كبريتيد الهيدروجين وفقاُ للمعادلة :
FeCl2 + H2S → FeS↓+ 2HCl
وعند إضافة حمض الهيدروكلوريك المركز يتجه التفاعل ناحية التفاعل العكسي ( اتجاة تكون كلوريد الحديدوز) حسب قاعدة لوشاتيليه وحسب قاعدة الأيون المشترك (-Cl) وحينها لا يمكن تمييز الراسب.
فلماذا ندخل فى كل هذه الموضوعات المتشابكة لذلك تم استخدام محلول هيدروكسيد الأمونيوم NH4OH وفي وجود كمية قليلة من محلول كلوريد الأمونيوم NH4Cl ليتم الكشف عن أيونات الحديدوز ليتكون راسب بنى مائل للاحمرار من هيدروكسيد الحديديك
وعند إضافة هيدروكسيد الأمونيوم لمحلول الملح نحصل على راسب أبيض مائل للخضرة دليل على وجود أيونات الحديدوز.