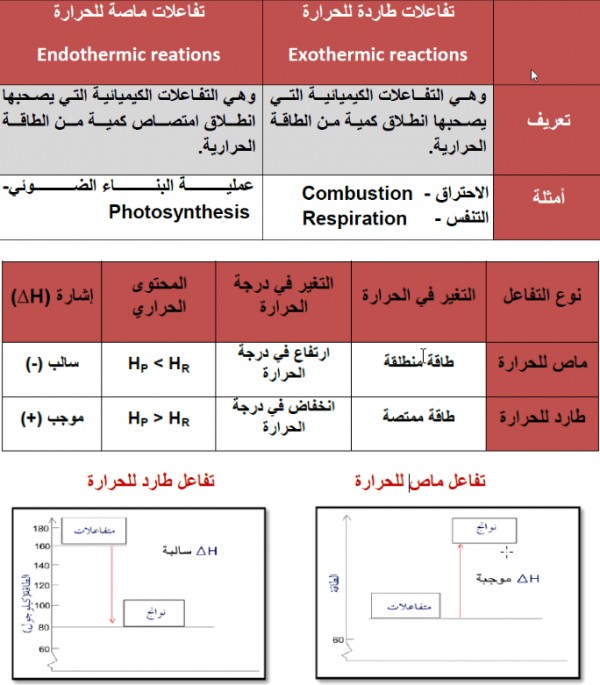
التفاعلات الطاردة للحرارة Exothermic reaction
(1) التفاعلات الطاردة للحرارة هى التفاعلات التى ينتج عنها طاقة حرارية كناتج من نواتج التفاعل إلى الوسط المحيط فترتفع درجة حرارته.
(2) تنتقل الطاقة الحرارية من النظام إلى الوسط المحيط مما يؤدي إلى انخفاض درجة حرارة النظام وارتفاع درجة حرارة الوسط المحيط.
(3) قيمة التغير فى المحتوى الحراري القياسي ΔHo تكون بإشارة سالبة لأن المحتوي الحراري للنواتج أقل من المحتوي الحراري للمتفاعلات.

(4) الشكل التالى يوضح مخطط الطاقة للتفاعلات الطاردة للحرارة.
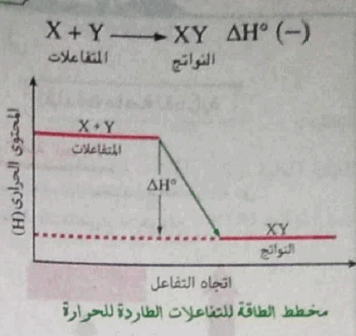
(5) مثال : تفاعل اتحاد غازي الهيدروجين والأكسجين لتكوين الماء
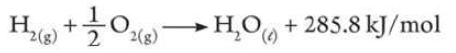
ويكون مخطط الطاقة لهذا التفاعل كالتالي:
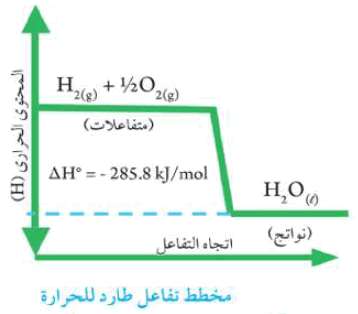
ملاحظة هامة:
التفاعلات الطاردة للحرارة تكون مصحوبة بانطلاق قدر من الطاقة الحرارية وذلك لان مجموع المحتوى الحراري للمواد الناتجة يكون أقل مما للمواد المتفاعلة وتبعاً لقانون بقاء الطاقة لابد من تعويض النقص في حرارة النواتج في صورة طاقة منطلقة.
التفاعلات الماصة للحرارة Endothermic reaction
(1) التفاعلات الماصة للحرارة هى التفاعلات التى يلزم لحدوثها امتصاص طاقة حرارية من الوسط المحيط فتنخفض درجة حرارته.
(2) تنتقل الطاقة الحرارية من االوسط المحيط إلى النظام مما يؤدي إلى ارتفاع درجة حرارة النظام وانخفاض درجة حرارة الوسط المحيط.
(3) قيمة التغير فى المحتوى الحراري القياسي ΔHo تكون بإشارة موجبة لأن المحتوي الحراري للنواتج أكبرمن المحتوي الحراري للمتفاعلات ، طبقاُ للمعادلة :

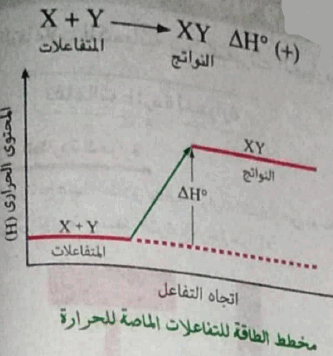
(4) الشكل التالى يوضح مخطط الطاقة للتفاعلات الماصة للحرارة.
(5) مثال : تفكك كربونات الماغنسيوم بالحرارة إلى أكسيد الماغنسيوم وغاز ثانى أكسيد الكربون.
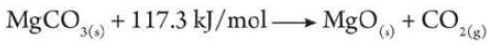
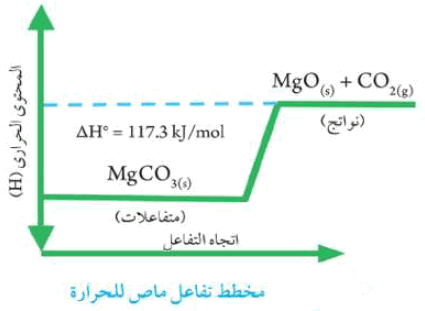
ويكون مخطط الطاقة لهذا التفاعل كالتالي:
ملاحظة هامة:
التفاعلات الماصة للحرارة تكون مصحوبة بامتصاص قدر من الطاقة الحرارية وذلك لان مجموع المحتوى الحراري للمواد الناتجة يكون أكبر مما للمواد المتفاعلة وتبعاً لقانون بقاء الطاقة لابد من تعويض النقص في حرارة المتفاعلات في صورة طاقة ممتصة.
مقارنة بين التفاعلات الطاردة للحرارة والتفاعلات الماصة للحرارة