أولاً/ عملية شحن البطارية
- هى عملية تزويد بالطاقة من مصدر خارجي.
- البطارية تعمل عند الشحن كخلية تحليلية تستهلك الطاقة من مصدر خارجي.
- يحدث تفاعل أكسدة واختزال غير تلقائي.
ثانياً/ عملية تفريغ البطارية
- هى عملية استهلاك الطاقة الكهربية المتولدة من البطارية.
- البطارية تعمل عند التفريغ كخلية جلفانية تنتج الطاقة الكهربية.
- يحدث تفاعل أكسدة واختزال غير تلقائي.
وسوف نشرح أدناه عملية شحن وتفريغ بطارية الرصاص الحامضية (بطارية السيارة) كمثال على ذلك
- الجدول التالي هو ملخص ما سبق:

شحن وتفريغ بطارية الرصاص الحامضية (بطارية السيارة)
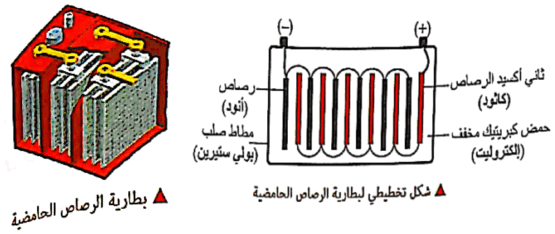
مكونات البطارية
(1) الأنود (المصعد): شبكة من الرصاص مملوءة برصاص إسفنجي (pb)
(2) المهبط (الكاثود): شبكة من الرصاص مملوءة بعجينة من ثاني اكسيد الرصاص (pbO2)
(3) إلكتروليت: محلول حمض الكبريتيك المخفف (H2SO4)
- تفصل ألواح الأنود والكاثود بصفائح عازلة.
- توضع المكونات في وعاء مصنوع من المطاط الصلب او البلاستيك (بولي سترين) لأنه لا يتأثر بالأحماض.
- تعمل البطارية كخلية جلفانية اثناء تشغيلها (تفريغها) واستهلاك طاقتها وتعمل كخلية إلكتروليتية عند إعادة شحنها.
تفاعلات التفريغ
- حيث تعمل الخلية كخلية جلفانية.
تُكتب أنصاف التفاعلات كالتالي:
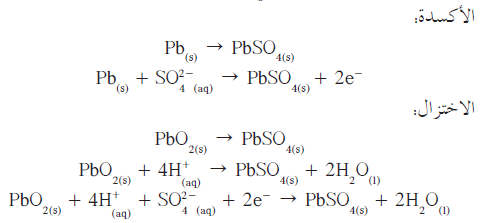
عند جمع معادلتي تفاعل الأكسدة والاختزال جمعًا جبريًّا نحصل على التفاعل النهائي للخليّة:
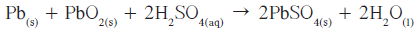
توضّح هذه المعادلة أنّ كبريتات الرصاص تتكوّن عند إغلاق الدائرة الخارجية للخليّة وتتراكم على الألواح ببطء فيقلّ تركيز حمض الكبريتيك وهذا ما يُسمّى عمليّة التفريغ .
تفاعلات الشحن
- تعمل الخلية كخلية تحليلية
يحدث التفاعل العكسي عند إعادة شحن المركم الرصاصي عن طريق دوران مولّد التيّار الكهربائي الموجود في السيارة مما يؤدي إلي:
(1) تحول كبريتات الرصاص إلى رصاص عند الآنود وثاني أكسيد الرصاص عند الكاثود.
(2) يعود تركيز الحمض إلى ماكان عليه
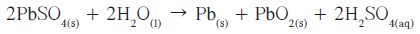
هذا التفاعل غير تلقائي ويتطلّب مرور تيّار كهربائي مستمرّ عبر خلايا المركم في عكس اتجاه التيّار الذي يمرّ أثناء عملية التفريغ.
- من الناحية النظرية ، يمكن تفريغ المركم الرصاصي وإعادة شحنه لعدد لا نهائي من المرّات ولكنّ عمره من الناحية العملية ، محدود ويرجع ذلك إلى ترسّب كميات صغيرة من كبريتات الرصاص في قاعه.
التفاعل الكلى للشحن والتفريغ:
