الأحماض الأمينية Amino acids
الأحماض الأمينية هي مجموعة من المركبات العضوية متكونة من مجموعة أمين (NH2-) على الأقل مشتبكة مع مجموعة كربوكسيل (COOH-)
- الصيغة العامة للأحماض الأمينية هي:
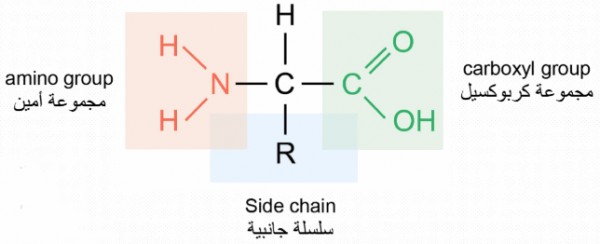
- تذوب الاحماض الامينية بصورة عامة في الماء.
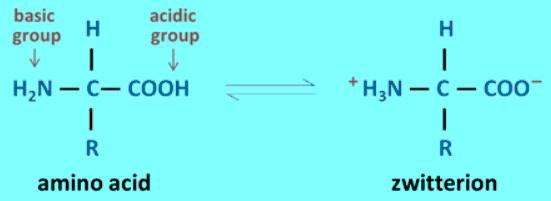
- يرجع معظم خواص الأحماض الأمينية إلى وجود الأيون المزدوج Zwitterions
- الأيون المزدوج هو شكل الحمض الأميني الناتج عن منح مجموعة الكربوكسيل فيه بروتونها لمجموعة الأمين.
كيف ترتبط الأحماض الأمينية بالماء
- عندما تذوب الأحماض الأمينية فى الماء فأن الأيون المزدوج Zwitterions يتفاعل مع الماء مرة كحمض ومرة أخرى كقاعدة.
(1) تفاعل الأيون المزدوج مع الماء وتصرفه كحمض
- مجموعة +NH3 حمض ضعيف وتتبرع بأيون الهيدروجين إلى جزئ الماء ولأنها حمض ضعيف فأن الأتزان سيتجه إلى اليسار.

(2) تفاعل الأيون المزدوج مع الماء وتصرفه كقاعدة
- مجموعة -COO قاعدة ضعيفة وتأخذ أيون الهيدروجين من جزئ الماء ولأنها قاعدة ضعيفة فأن الأتزان سيتجه إلى اليسار.

الخلاصة
- عند ذوبان الحمض الأمينى فى الماء فأنه يحدث كلا التفاعلين السابقين.
- ولكن موضع الأتزان فى كلا التفاعلين يكون غير متطابق وهذا يعتمد على تأثير المجموعة الجانبية "R"
- بالنسبة للأحماض الأمينية البسيطة فأن وضع الاتزان الأول سيتجه الى حد ما إلى اليمين عن الاتزان التاني.
- وهذا يعنى أن الأيونات السالبة (من الحمض الأميني) فى المحلول ستكون أكبر الى حد ما من الأيونات الموجبة.