الوزن الجزيئي لأى مركب
- الوزن الجزيئي هو مجموع وزن كل الذرات في صيغة جزيئية معطاة.
- يقاس الوزن الجزيئي بوحدة الكتل الذرية، ويعبر عنها عادةً برمز u أو .amu .
- لحساب الوزن الجزيئي لصيغة كيميائية، ستحتاج لجمع الأوزان الذرية لكل عنصر موجود.
- الوزن الجزيئي يسمى فى بعض الكتب بكتلة الصيغة Formula weight
خطوات حساب الوزن الجزيئي
(1) عد مجموع ذرات كل عنصر في الجزيء. اكتب كل عنصر موجود في الجزيء. يمكنك استخدام الرمز الكيميائي أو كتابة اسم العنصر، ثمّ عد الذرات طبقًا للصيغة الجزيئية واكتب عدد كل ذرة بجانب اسم العنصر أو رمزه.
(2) اعثر على قيمة الوزن الذري التقريبي لكل عنصر في الجزيء. استخدم نسخة من الجدول الدوري للعناصر. يعرض الجدول الدوري الكتلة الذرية لكل عنصر أسفل الرمز الكيميائي. تبلغ الكتلة الذرية للأكسجين على سبيل المثال 15.9994 amu (أي وحدة الكتل الذرية)
(3) احسب الكتلة الكلية لكل عنصر في الجزيء. اضرب الكتلة الذرية لكل عنصر في عدد ذرات ذلك العنصر كالتالي: (الكتلة الذرية للعنصر) x (عدد ذرات هذا العنصر). قم بذلك لكل عنصر في الجزيء.
(4) اجمع كتلة كل الذرات لإيجاد الوزن الجزيئي الكلي للجزيء.
(5) قرّب الناتج عند الضرورة باستخدام أرقام عشرية منتهية.
- تذكّر استخدام الوحدات الصحيحة. amu هو الاختصار القديم لوحدة الكتل الذرية، ولكن حديثًا أصبح رمز u –وهو حرف u إنجليزي صغير- هو الأكثر صحةً كوحدة للكتلة الذرية.
مثال (1): احسب الوزن الجزيئى للمركب Fe(OH)3.12H2O؟
- الكتلة الذرية للحديد = 55.85 amu
- الكتلة الذرية للأكسجين= 16 amu
- الكتلة الذرية للهيدروجين= 1 amu
يمكن الحصول على هذة الكتل الذرية من الجدول الدوري
الوزن الجزيئي = مجموع الكتلة الذرية لكلعنصر موجود فى الصيغة الجزيئية X عدد تواجده فى الصيغة
373.58 = (Fe(OH)3.12H2O = 55.58 + (16+1)*3 +12(1*2+16
مثال (2)

الحل:
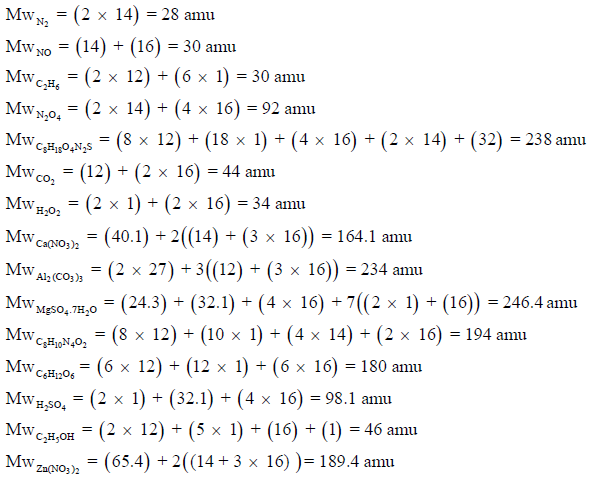
الكتلة المولية Molar Mass
- كتلة المول من المادة ( الكتلة المولية) هو الكتلة الجزيئية لهذة المادة معبرة عنها بالجرامات.
- أول من أطلق اسم (مول) هو العالم فيلهلم أوستفالد عام 1894م وهي مشتقة من الكلمة الألمانية Mol وهو تكبير لكلمة Molecule أى جزئ.
مثال: أحسب مول واحد من كلوريد الكالسيوم
كتلة المول الواحد من كلوريد الكالسيوم CaCl2 = الكتلة الجزيئية لكلوريد الكالسيوم معبراً عنها بالجرامات
الكتلة الجزيئية لكلوريد الكالسيوم = ( 2 * كتلة أيون الكلوريد) + (1 * كتلة أيون الكالسيوم)
الكتلة الذرية للكلور = 35.5amu ، والكتلة الذرية للكالسيوم = 40amu
الكتلة الجزيئية لكلوريد الكالسيوم =
( 2 * 35.5) + (1 * 40) = 111amu
كتلة المول الواحد من كلوريد الكالسيوم CaCl2 يساوي 111g
مصادر / مراجع مهمة عن الوزن الجزيئي
(1) كتاب مبادئ الكيمياء العامة (نظري + مسائل محلولة) كتلة الصيغة ص59
(2) الكتاب الشامل فى الكيمياء العامة باللغة العربية الفصل الأول / طرق التعبير عن التركيز- ص 18