تفاعلات الإحلال المزدوج
- يسمى التفاعل الذي يتم فيه تبادل الأيونات بين مركبين تفاعل الإحلال المزدوج.
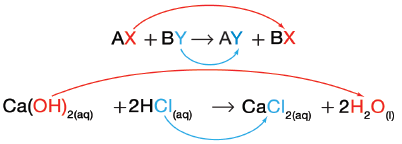
- يمثل الرمزان B , A في هذة المعادلة أيونين موجبين بينما يمثل الرمزان X , Y أيونين سالبين. لاحظ أن الأيونين السالبين قد تبادلا موقعيهما، وصارَا مرتبطين بأيونين موجبين مختلفين.
- بمعنى آخر حل X محل Y ، وحل Y محل X ولهذا السبب يسمى التفاعل تفاعل الإحلال المزدوج.
أمثلة توضيحية
(1) تفاعل هيدروكسيد الكالسيوم وحمض الهيروكلوريك
(Ca(OH)2(aq) + 2HCl(aq) → CaCl2(aq) + 2H2O(l
الأيونات في التفاعل هي: -Ca2+ , -OH , H+ , Cl
لاخظ أن الأيونين السالبين: Cl- ، -OH قد غيرا موقعهما ، وارتبطا بالأيونين الموجبين +Ca2+ , H على الترتيب.
(2) تفاعل هيدروكسيد الصوديوم مع كلوريد النحاس II
(2NaOH(aq) + CuCl2(aq) → 2NaCl(aq) + Cu(OH)2(s
لاحظ أن الأيونين السالبين: Cl- ، -OH قد غيرا موقعهما ، وارتبطا بالأيونين الموجبين +Na+ , Cu2 على الترتيب.
- ناتج هذا التفاعل مادة صلبة لا تذوب في الماء وهي هيدروكسيد النحاس II وتسمى المادة الصلبة التى تنتج خلال تفاعل كيميائي في محلول ما راسباً.

الخطوات الأساسية لكتابة المعادلات الكيميائية الموزونة لتفاعلات الإحلال المزدوج

فوائد تفاعلات الإحلال المزدوج
- إحدى المميزات الأساسية لتفاعلات الإحلال المزدوج هى نوع الناتج المتكون عندما يحدث التفاعل، فجميع هذه التفاعلات تنتج ماءً أو راسباً أو غازاَ.
(1) أحدى النواتج ماء
(Ca(OH)2(aq) + 2HCl(aq) → CaCl2(aq) + 2H2O(l
(2) أحدى النواتج راسب
↓ (2NaOH(aq) + CuCl2(aq) → 2NaCl(aq) + Cu(OH)2 (s
(3) أحدي النواتج غاز
(KCN(aq) + HBr(aq) → KBr(aq) + HCN(g