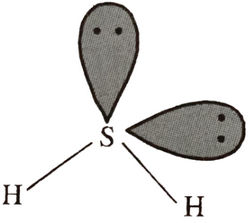
المجموعات الإلكترونية حول الذرة المركزية
- يَشمل شكل أزواج الإلكترونات حول الذرّة المركزية على جميع المجموعات الإلكترونية الرابطة وغير الرابطة، أما شكل الجزيء فيشمل فقط ترتيب الذرات حول الذرة المركزية.
- تُعامل إلكترونات الرابطة الواحدة، سواء كانت أحادية أو ثنائية أو ثلاثية على أنّها مجموعة واحدة من الإلكترونات.
- الجدول التالي عدد المجموعات الإلكترونية حول الذرّة المركزية لبعض الجُزيئات
مثال (1): أحسب عدد المجموعات الإلكترونية فى OF2 , NH3
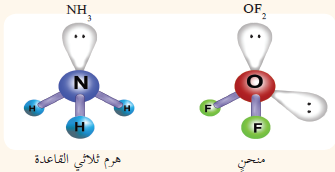
شكل لويس لكل منهما كالتالي:

- يَتضح من شكل لويس وجود أربع مجموعات إلكترونية حول الذرّة المركزية في كلا الجزيئين.
- حيث يوجد في جزيء OF2 مجموعتان من الإلكترونات الرابطة، ومجموعتان من الإلطترونات غير الرابطة.
- بينما يوجد في جزيء NH3 ثلاث مجموعات إلكترونية رابطة، ومجموعة إلكترونية واحدة غير رابطة، وحسب نظرية تنافر أزواج إلكترونات التكافؤ، فإنّ شكل الأزواج الإلكترونية في كل منهما رباعي الأوجه.
مثال (2): ما هو عدد المجموعات الالكترونية الموجودة في H2S؟
- شكل لويس لمركب كبريتيد الهيدروجين كالتالي:
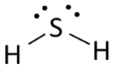
- يتضح من شكل لويس وجود أربع مجموعات إلكترونية حول الذرة المركزية (الكبريت).
- حيث يوجد في جزيء كبريتيد الهيدروجين H2S مجموعتان من الإلكترونات الرابطة ( التى تكون الروابط)، ومجموعتان من الإلكترونات غير الرابطة (أزواج الألكترونات على ذرات الكبريت).