النسبة المئوية للمذاب بالكتلة
ويكمن تعريفها كالتالي:
(1) هي النسبة المئوية بين كتلة المذاب وكتلة المحلول.
(2) أو كتلة المادة المذابة مقاسه بالجرامات الموجودة في مائة جرام من المحلول
(3) أو عدد الجرامات من المذاب فى 100g من المحلول.
- وتعطى من العلاقة التالية:
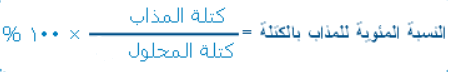
علماً بأن : كتلة المحلول = كتلة المذاب + كتلة المذيب.
أمثلة محلولة
مثال (1): محلول هيدروكسيد الصوديوم NaOH تركيزه 10% ماذا تعني لك هذه النسبة ؟
الحل:
تعني أن كتلة هيدروكسيد الصوديوم 10% من كتلة المحلول .
أي أن كل 100gmمن المحلول يتكون من :
NaOH → 10gm
H2O → 90gm
مثال (2): ماهي كتلة كلوريد البوتاسيوم وما حجم الماء اللازم لتحضير 250 غرام من محلول تركيزه 3%؟
الحل:
النسبة المئوية بالكتلة = 3%
كتلة المذاب (كلوريد البوتاسيوم) = ؟؟ جم
كتلة المذيب (الماء) = ؟؟ جم
كتلة المحلول = كتلة المذاب (كلوريد البوتاسيوم) + كتلة المذيب (الماء) = 250 جم
وبالتعويض فى القانون السابق يكون:
3% = (كتلة كلوريد البوتاسيوم / 250) * 100
كتلة كلوريد البوتاسيوم = 7.5 جم
وبما أن :
كتلة المحلول = كلوريد البوتاسيوم + كتلة الماء
250 = 7.5 + كتلة الماء
كتلة الماء = 242.5 جم