+BF3 & GaI3 & BI3 & SO3 & CO3-- & NO3- & CH3
Щ…Ш«Ш§Щ„ (1): Ш«Ш§Щ„Ш« ЩҒЩ„ЩҲШұЩҠШҜ Ш§Щ„ШЁЩҲШұЩҲЩҶ BF3
- ШӘШұЩғЩҠШЁ Щ„ЩҲЩҠШі:

ЩҶЩ„Ш§ШӯШё Ш§ЩҶ ШӯЩҖЩҲЩ„ Ш§Щ„Ш°ШұШ© Ш§Щ„Щ…ШұЩғШІЩҠШ© Ш«Щ„Ш§Ш«Ш© Ш§ШІЩҲШ§Ш¬ ШҘЩ„ЩғШӘШұЩҲЩҶЩҠШ© ШұШ§ШЁШ·Ш© ШҢ ЩҲШЁШ°Щ„Щғ ШӘШӘЩҲШІШ№ ЩҮШ°ЩҮ Ш§Щ„ШҘЩ„ЩғШӘШұЩҲЩҶШ§ШӘ ШЁШӯЩҠШ« ШӘЩғЩҲЩҶ ШЈШЁШ№ШҜ Щ…Ш§ ЩҠЩ…ЩғЩҶ Ш№ЩҶ ШЁШ№Ш¶ЩҮШ§ Ш§Щ„ШЁШ№Ш¶ ШҢ ШЁШӯЩҠШ« ШӘЩӮЩ„Щ„ Щ…ЩҶ ШЈШ«Шұ Ш§Щ„ШӘЩҶШ§ЩҒШұ ШЁЩҠЩҶЩҮШ§ Щ„ШӘШөШЁШӯ ЩҒЩҠ ШЈШұЩғШ§ЩҶ Щ…Ш«Щ„Ш« Щ…ШӘШіШ§ЩҲЩҠ Ш§Щ„ШЈШ¶Щ„Ш§Ш№ Щ…ШұЩғШІЩҮ Ш°ШұШ© Ш§Щ„ШЁЩҲШұЩҲЩҶ ШҢ ЩҲШӘЩғЩҲЩҶ Ш§Щ„ШІШ§ЩҲЩҠШ© ( (F B F) ШӘШіШ§ЩҲЩҠ 120o

Щ…Щ„Ш§ШӯШёШ© ЩҮШ§Щ…Ш© : ШӘШ№Ш§Щ…Щ„ Ш§Щ„ШұЩҲШ§ШЁШ· Ш§Щ„Щ…Ш¶Ш§Ш№ЩҒШ© Ш§ЩҲ Ш§Щ„Ш«Щ„Ш§Ш«ЩҠШ© Щ…Ш№Ш§Щ…Щ„Ш© Ш§Щ„ШұЩҲШ§ШЁШ· Ш§Щ„ШЈШӯШ§ШҜЩҠШ© Щ„ШЈЩҶ Ш§Щ„ШұШ§ШЁШ·Ш© Ш§Щ„ШЈШӯШ§ШҜЩҠШ© ШЈЩҲ Ш§Щ„Ш«ЩҶШ§ШҰЩҠШ© ШЈЩҲ Ш§Щ„Ш«Щ„Ш§Ш«ЩҠШ© ШЁЩҠЩҶ Ш§Щ„Ш°ШұШӘЩҠЩҶ ШӘШҙШәЩ„ ЩҶЩҒШі Ш§Щ„Щ…ЩҶШ·ЩӮШ© Щ…ЩҶ Ш§Щ„ЩҒШұШ§Шә
(2) ШІШ§ЩҲЩҠ (Щ…ЩҶШӯЩҶЩҠ) Angular ШЈЩҲ ШҙЩғЩ„ V - Shape V ШЈЩҲШәЩҠШұШ®Ш·ЩҠ non -Linear
- ЩҮШ°ЩҮ Ш§Щ„Щ…ШұЩғШЁШ§ШӘ ЩҠШұЩ…ШІ Щ„ЩҮШ§ ШЁЩҖ AX2E ШЈЩҠ ШЈЩҶ Ш§Щ„Ш°ШұШ© Ш§Щ„Щ…ШұЩғШІЩҠШ© A ШӘШұШӘШЁШ· ШЁШ°ШұШӘЩҠЩҶ 2X ЩҲШІЩҲШ¬ ШәЩҠШұ ШұШ§ШЁШ· (ШӯШұ) E.
- ШЈЩҠ ШЈЩҶ Ш§Щ„Ш°ШұШ© Ш§Щ„Щ…ШұЩғШІЩҠШ© ШӘШұШӘШЁШ· ШЁШІЩҲШ¬ЩҠЩҶ ШұШ§ШЁШ·ЩҠЩҶ (ШЈЩҲ Щ…Ш¬Щ…ЩҲШ№ШӘЩҠЩҶ Щ…ЩҶ Ш§Щ„ШЈШІЩҲШ§Ш¬ Ш§Щ„ШұШ§ШЁШ·Ш©) ЩҲШІЩҲШ¬ ШӯШұ.
- ЩҲЩҒЩҠ ЩҮШ°ЩҮ Ш§Щ„ШӯШ§Щ„Ш© ШӘЩғЩҲЩҶ Ш§Щ„ШІШ§ЩҲЩҠШ© ШЁЩҠЩҶ Ш§Щ„ШұЩҲШ§ШЁШ· (X AX) Ш§ЩӮЩ„ Щ…ЩҶ 120o .
- ЩҲЩ…ЩҶ Ш§Щ„ШЈЩ…Ш«Щ„Ш© Ш№Щ„Щү ЩҮШ°Ш§ Ш§Щ„ЩҶЩҲШ№ :
-SO2 & SnCl2 & PbF2 & NOCl & NO2- & BH2
Щ…Ш«Ш§Щ„(1): ЩғЩ„ЩҲШұЩҠШҜ Ш§Щ„ЩӮШөШҜЩҠШұ SnCl2
- ШӘШұЩғЩҠШЁ Щ„ЩҲЩҠШі ЩҮЩҲ:
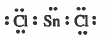
ЩҶЩ„Ш§ШӯШё Ш§ЩҶ ШӯЩҖЩҲЩ„ Ш§Щ„Ш°ШұШ© Ш§Щ„Щ…ШұЩғШІЩҠШ© ШІЩҲШ¬ЩҠЩҶ ШұШ§ШЁШ·ЩҠЩҶ ЩҲШІЩҲШ¬ ШӯЩҖШұШҢ ЩҲШЁШ°Щ„Щғ ШӘШӘЩҲШІШ№ ЩҮШ°ЩҮ Ш§Щ„ШҘЩ„ЩғШӘШұЩҲЩҶШ§ШӘ ШЁШӯЩҠШ« ШӘЩғЩҲЩҶ ШЈШЁШ№ШҜ Щ…Ш§ ЩҠЩ…ЩғЩҶ Ш№ЩҶ ШЁШ№Ш¶ЩҮШ§ ШЁШӯЩҠШ« ШӘЩӮЩ„Щ„ Щ…ЩҶ ШЈШ«Шұ Ш§Щ„ШӘЩҶШ§ЩҒШұ ШЁЩҠЩҶЩҮШ§ Щ„ШӘШӘЩҲШІШ№ ЩҒЩҠ ШЈШұЩғШ§ЩҶ Щ…Ш«Щ„Ш« Щ…ЩҖШіЩҖШӘЩҖЩҲ ЩҲШӯЩҖЩҠШ« ШЈЩҶ Ш§Щ„ШҙЩғЩ„ Ш§Щ„ЩҮЩҶШҜШіЩҠ Щ„Щ„ЩҖШ¬ЩҖШІЩҠШЎ ЩҠЩҖШӯЩҖЩҖШҜШҜЩҮ ШЈЩ…ЩҖШ§ЩғЩҶ Ш§Щ„Ш°ШұШ§ШӘ ЩҲЩ„ЩҠШі ШЈЩ…Ш§ЩғЩҶ Ш§Щ„ШЈШІЩҲШ§Ш¬ Ш§Щ„ШҘЩ„ЩғШӘШұЩҲЩҶЩҠШ©ШҢ Щ„Ш°Ш§ ЩҒШҘЩҶ Ш§Щ„ШҙЩғЩ„ Ш§Щ„ЩҮЩҶШҜШіЩҠ Ш§Щ„ШөЩҖШӯЩҖЩҠЩҖШӯ Щ„Щ„Ш¬ЩҖШІЩҠШЎ ЩҮЩҲ ШҙЩғЩ„ ШІШ§ЩҲЩҠ ( Щ…ЩҶШӯЩҶЩҠ ) ( ШәЩҠШұ Ш®Ш·ЩҠ) ( ШҙЪ©Щ„ V).

Щ…Щ„Ш§ШӯШёШ© ЩҮШ§Щ…Ш©: ЩҠШ®ШӘЩ„ЩҒ ЩҮШ°Ш§ Ш§Щ„ШҙЩғЩ„ Ш№ЩҶ Ш§Щ„ШҙЩғЩ„ ( Щ…Ш«Щ„Ш« Щ…ШіШӘЩҲ ) ШЁШ§ЩҶ Ш§Щ„ШІШ§ЩҲЩҠШ© (Cl Sn Cl) Ш§ЩӮЩ„ Щ…ЩҶ В°120 ЩҲШ°Щ„Щғ Щ„ЩҲШ¬ЩҲШҜ ШІЩҲШ¬ ШӯЩҖШұ (ШәЩҠШұ ШұШ§ШЁШ· ) Ш§Щ„Ш°ЩҠ ЩҠЩ…ШӘЩ„Щғ Ш·Ш§ЩӮШ© ШЈШ№Щ„Щү ЩҲШЁШ°Щ„Щғ ЩҠШіШЁШЁ ШӘЩҶШ§ЩҒШұ ШЈЩғШЁЩҖШұ ШҢ ЩҲЩ„ЩҮШ°Ш§ ШӘШЁШӘШ№ШҜ Ш№ЩҶЩҮ Ш§Щ„ШЈШІЩҲШ§Ш¬ Ш§Щ„ШұШ§ШЁШ·Ш© ШҢ ЩҲШЁШ°Щ„Щғ ШӘЩӮЩ„ Ш§Щ„ШІШ§ЩҲЩҠШ© Ш№ЩҶ В°120 ШҢ ЩҮШ°Ш§ Щ…ЩҶ ШӯЩҠШ« Ш§Щ„ШІШ§ЩҲЩҠШ© ШҢ ШЈЩ…Ш§ Щ…ЩҶ ШӯЩҠШ« Ш§Щ„Ш°ШұШ§ШӘ ЩҒШ§Щ„Щ…Ш«Щ„Ш« Ш§Щ„Щ…ШіШӘЩҲ ЩҠШӯШӘЩҲЩҠ Ш№Щ„Щү Ш«Щ„Ш§Ш« Ш°ШұШ§ШӘ ШӘШӯЩҠШ· ШЁШ§Щ„Ш°ШұШ© Ш§Щ„Щ…ШұЩғШІЩҠШ© ШЈЩ…Ш§ Ш§Щ„ШҙЩғЩ„ ШәЩҠШұ Ш§Щ„Ш®Ш·ЩҠ ЩҒЩҠШӯШӘЩҲЩҠ Ш№Щ„Щү Ш°ШұШӘЩҠЩҶ ШӘШӯЩҠШ· ШЁШ§Щ„Ш°ШұШ© Ш§Щ„Щ…ШұЩғШІЩҠШ© .