التدرج في الحجم الأيوني
- ذرات العناصر الفلزية لها طاقات تأين منخفضة، وهي تكوّن أيونات موجبة بسهولة.
- وعلى النقيض من ذلك، فإنّ ذرّات عناصر اللافلزات لها طاقات تأين عالية.
- دعنا نوضح الآن كيف يؤثر فقد أو اكتساب إلكترونات على حجم الأيون المتكوّن.
تدرج الحجم الأيوني في المجموعات
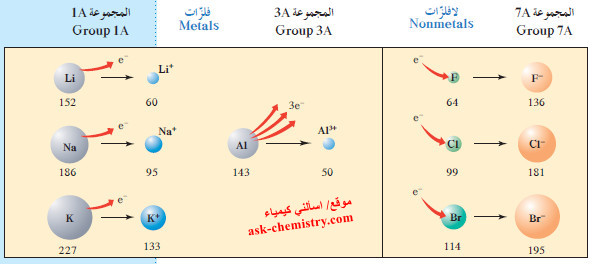
- تكون الأيونات الموجبة (الكاتيونات) دائمًا أصغر حجمًا من الذرات المتعادلة التي تتكوّن منها ، وذلك بسبب فقدان إلكترونات من الغلاف الخارجي للذرّة ما ينتج عنه زيادة الجذب بواسطة النواة للإلكترونات المتبقية.
- كما ترى في الشكل لتالي: يساوي نصف قطر ذرّة الصوديوم 186pm Na، حوالی ضعف نصف قطر كاتيون الصوديوم +95pm Na. ونصف قطر كاتيون الألمنيوم 3+A1 يساوي فقط 1/3 نصف قطر ذرّة الألمنيوم.
- على النقيض من ذلك ، نجد أن الأيونات السالبة (الأنيونات) تكون دائمًا أكبر حجمًا من الذرّات المتعادلة المتكونة منها، وذلك لأن قوة جذب شحنة النواة الفعّالة تصبح أقل لزيادة عدد الإلكترونات.
- يساوي نصف قطر أنيون الكلوريد -181pm Cl حوالي ضعف نصف قطر ذرّة الكلور 99pm Cl .
- يوضح الشكل التدرّج في أنصاف الأقطار الذرية، وأيضًا التدرّج في الحجم الأيوني تجاه المجموعة لبعض عناصر المجموعات 1A ، 3A و 7A.
تدرج الحجم الأيوني في الدورات
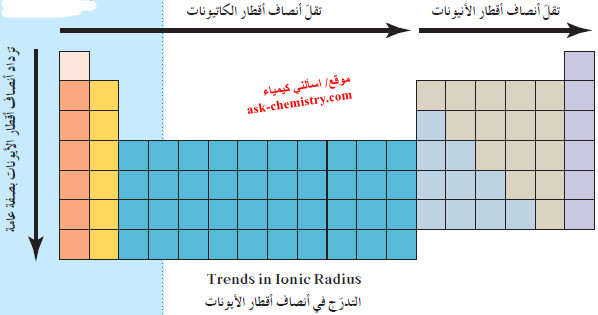
- يوضح الشكل التالي العلاقة الدورية لأنصاف أقطار العناصر، حيث يحدث نقص تدريجي لحجم الأيونات الموجبة كلّما اتجهنا من اليسار إلى اليمين عبر الدورة.
- بدءاً بالمجموعة 5A ، حيث توجد الأيونات السالبة الأكبر بكمية أكبر من الأيونات الموجبة ، نلاحظ أيضًا نقصًا تدريجيًّا في الحجم كلّما تحرّكنا إلى اليمين عبر الدورة .
- تتزايد أنصاف أقطار الأنيونات والكاتيونات كلما اتجهنا إلى أسفل في كل مجموعة.
كلما
- يوضح الشكل التالي التدرّج في الحجم الأيوني في كلّ من المجموعات والدورات.