تأثير الأيون المشترك Common ion effect
- هو تأثير وجود زيادة في المحلول من إحدى شوارد الألكتروليت ضعيف الانحلال.
- يمكن توقع نتيجة تأثير هذا التغير من مبدأ لوشاتلييه الذي ينص على أنه عند تطبيق مؤثر على نظام متزن فإن الاتزان سينزاح بالاتجاه الذي يميل إلى تخفيف ذلك المؤثر أو إلغائه.
- سنوضح ذلك بالأمثلة التالية:
مثال (1): عند إضافة غاز كلوريد الهيدروجين إلى محلول مشبع من كلوريد الصوديوم
(أ) في البداية يتأين كلوريد الصوديوم إلى أيونات الكلوريد وأيونات الصوديوم ويكون النظام فى حالة إتزان كما بالمعادلة:
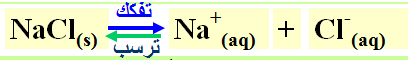
(ب) عند إضافة كلوريد الهيدروجين إلى النظام فأنه يتأين بشكل كامل وتتكون أيونات الكلوريد وأيونات الهيدرونيوم كما بالمعادلة:
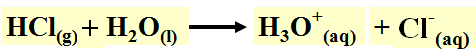
ملاحظات
(1) الأيون المشترك فى المعادلتين هو أيون الكلوريد -Cl
(2) عند أضافة HCl لمحول الملح NaCl فهل يترسب الملح أم يذوب المزيد منه ؟ الملح يترسب
(3) هل يزداد تأين الملح أم يقل ؟ يقل التأين
التفسير:
عند إضافة كلوريد الهيدروجين لمحلول كلوريد الصوديوم يتزاح التفاعل إلى الاتجاه العكسي وهو إتجاه ترسيب كلوريد الصوديوم
وذلك حسب قاعدة لوشاتيليه التى تنص على "عند تطبيق مؤثر(أضافة أيونات الكلوريد من HCl) على نظام متزن (تأين NaCl) فإن الاتزان سينزاح بالاتجاه الذي يميل إلى تخفيف ذلك المؤثر أو إلغائه (اتجاة التفاعل العكسي: أتجاة ترسيب NaCl).
إذاً ما تأثير الأيون المشترك ؟
(1) يسبب الترسب (2) يقلل التأين
مثال (2): إضافة قليل من ملح CH3COONa إلى محلول CH3COOH
(أ) في البداية يتأين حمض الأستيك إلى أيونات الأسيتات وأيونات الهيدرنيوم ويكون النظام فى حالة إتزان كما بالمعادلة:
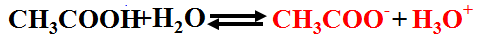
(ب) عند إضافة أستات الصوديوم إلى النظام فأنه يتأين بشكل تام وتتكون أيونات الأسيتات وأيونات الصوديوم كما بالمعادلة:
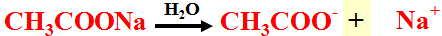
ملاحظات
(1) الأيون المشترك فى المعادلتين هو أيون الأسيتات -CH3COO
(2) عند أضافة اسيتات الصوديوم لحمض الأستيك ففى أى اتجاه ينزاح الاتزان؟ الأتجاة العكسي
(3) ماذا يحدث لتركيز حمض الأستيك ؟ يزداد التركيز وتزداد pH لأن التفاعل يسير فى الاتجاه العكسي وهو تكون الحمض
(4) هل يزداد تأين الحمض أم يقل ؟ يقل التأين لأن التفاعل يتجه نحو التفاعل العكسي وهو تكون الحمض
التفسير:
عند إضافة أسيتات الصوديوم لمحلول حمض الأستيك يتزاح التفاعل إلى الاتجاه العكسي وهو إتجاه تكون الحمض.
وذلك حسب قاعدة لوشاتيليه التى تنص على "عند تطبيق مؤثر(أضافة أيونات -CH3COO) على نظام متزن (تأين CH3COOH) فإن الاتزان سينزاح بالاتجاه الذي يميل إلى تخفيف ذلك المؤثر أو إلغائه (اتجاة التفاعل العكسي: أتجاة تكون الحمض CH3COOH).
إذاً ما تأثير الأيون المشترك ؟
(1) ازاحة الأتزان نحو التفاعل العكسي (2) يقلل التأين