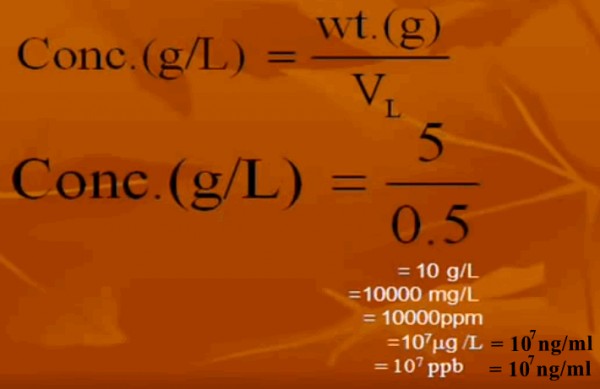تركيز المحلول
- يعبر عن النسبة بين كمية المذاب وحجم المحلول.
- القانون العام لحساب تركيز المحاليل :
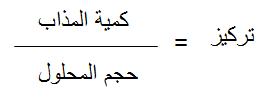
- وفى حالة التعبير عن كمية المذاب بالجرامات وحجم المحلول باللتر وهى الطرق الشائعة فى المعامل الكيميائية يستخدم القانون التالي:
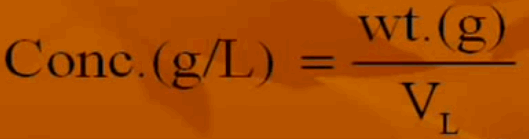
- وهنا تكون وحدة التركيز بــ g/L
- المطلوب هو إيجاد تركيز المادة بوحدة ng/ml
1g = 109 ng
1L = 103 ml
بالتعويض فى القانون السابق نحصل على :
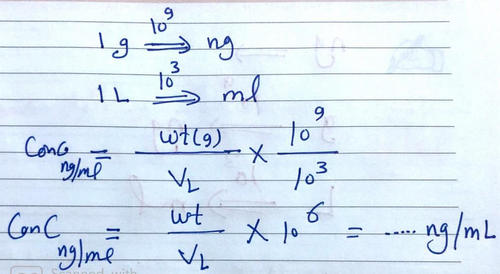
طريقة أخري للحل
- النانو جرام / ملليتر يكافئ وحدة ppb أى جزء لكل بليون جزء = Part per billion
1ng/ml = 1 ppb
لذلك نقوم بحساب التركيز بوحدة ppb
حساب التركيز بـــ ppb
- ppb : تعنى جزء لكل بليون جزء أى part per billion
- ppb : هو كتلة المذاب بالميكروجرام المذابة في 1 لتر من المذيب.
- ppb = μg /L
- الصيغة الرياضية للقانون:
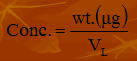
ويكون وحدة التركيز هنا هي
μg/L = ppb = ng/ml
مسألة محلولة
حضر محلول من كلوريد الصوديوم بإذابة 5g في 500ml من الماء المقطر ... عبر عن تركيز المحلول بوحدة g/L , ppm , ppb , ng/ml