حرارة التخفيف القياسية standard Heat of dilution
- تعرف كمية الحرارة المنطلقة أو الممتصة نتيجة زيادة كمية المذيب (التخفيف) باسم حرارة التخفيف القياسية ΔHodil
- حرارة التخفيف القياسية ΔHodil :
هي كمية الحرارة المنطلقة أو الممتصة لكل مول من المذاب عند تخفيف المحلول من تركيز أعلى إلى تركيز أقل وهو فى الظروف القياسية.
- ما معنى أن حرارة التخفيف القياسية لمحلول هيدروكسيد الصوديوم 4.5kJ/mol - ؟
أى أن كمية الحرارة المنطلقة لكل واحد مول من هيدروكسيد الصوديوم عند تخفيف المحلول من تركيز أعلى إلى تركيز أقل فى الظروف القياسية تساوي 4.5kJ
تفسير مصدر حرارة التخفيف
- تتم عملية التخفيف على خطوتين متعاكستين فى الطاقة وهما:
(1) عملية أبعاد أيونات أو جزيئات المذاب
تتم عملية أبعاد الأيونات عن بعضها فى المحلول الأعلى تركيزاً وتحتاج إلى امتصاص طاقة (عملية ماصة للحرارة)
(2) عملية ارتباط أيونات أو جزيئات المذاب
تتم عملية ارتباط الأيونات أو جزيئات المذاب بعدد أكبر من جزيئات المذيب وينتج عنها انطلاق طاقة (عملية طاردة للحرارة)
- ويمثل المجموع الجبري لطاقتي الأبعاد والأرتباط بقيمة حرارة التخفيف.
ملاحظات هامة :
(1) بزيادة كمية المذيب تزداد كمية الحرارة المنطلقة أو الممتصة
عند إذابة 1mol من هيدروكسيد الصوديوم الصلب في كميات مختلفة من الماء فأن حرارة الذوبان تختلف باختلاف كمية الماء (المذيب) كما يتضح من المعادلتين التاليين:
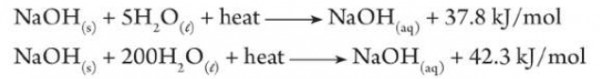
(2) يصاحب عملية التخفيف في بدايتها امتصاص طاقة
لأن زيادة جزيئات الماء أثناء عملية التخفيف تعمل على إبعاد أيونات أو جزيئات المذاب عن بعضها فى المحلول الأعلى تركيزاُ مما يحتاج امتصاص قدراً من الطاقة.