حمضية وقاعدية الكحولات ومقارنتها بالماء
(1) تسلك الكحولات سلوكاً مشابهاً لسلوك الماء من حيث الحمضية والقاعدية فهي تسلك سلوك كل من الحوامض الضعيفة والقواعد الضعيفة.
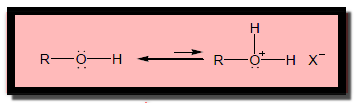
(أ) الكحولات كقواعد : تكتسب الكحولات البروتون بواسطة الأحماض القوية وتتكون ايونات +Oxonium – ROH2
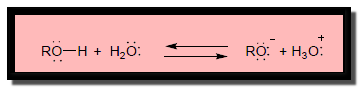
(ب) الكحولات كحوامض : تتفكك فى المحاليل المائية وتعطي أيون الهيدرونيوم وأيون -Alkoxide – RO
(2) عند مقارنة قيم ثابت التفكك لكل من الماء وأبسط الكحولات مثل الإيثانول والميثانول يتضح التشابة الكبير بين الماء والكحولات

المركبات التي تملك قيم Ka صغيرة تكون أحماض ضعيفة والعكس صحيح
(3) إن تأثير مجموعات الألكيل على حامضية الكحولات يعتمد على قدرة المذيب في تثبيت أيون alkoxide فمثلاً الأيون الأكثر ذوبانية فى الماء هو الأكثر ثباتاً فيه وبالتالي يكون الأعلى حمضية.
مثال: المركبات Methanol , Ethanol , tert-Butyl alcohol نجد أن الميثانول هي الأعلى كونه الأعلى ذوبانية في الماء.

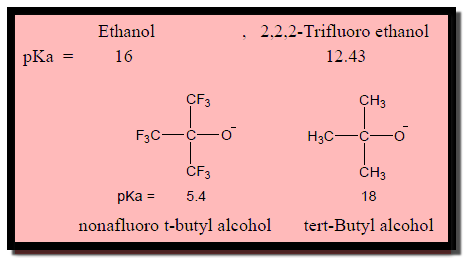
(4) المجموعات الساحبة للألكترونات تأثير هام على حمضية الكحولات حيث يعمل على تثبيت أيون Alkoxide وتكون pKa منخفضة
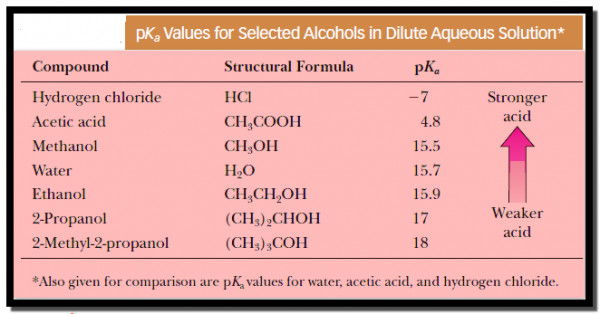
- الجدول التالي يوضح قيم pKa لبعض الكحولات في المحاليل المائية المخففة مقارنة ببعض المركبات الأخرى مثل الماء وحمض الهيدروكلوريك وحمض الخليك