الرابطة الهيدروجينية Hydrogen Bond
- تنشأ الرابطة الھیدروجینیة بین الجزیئات ثنائیة القطب بشكل خاص عندما ترتبط ذرة الھیدروجین تساھمیاً مع عنصر صغیر جداً ذي سالبیة كھربیة عالیة مثل :الفلور، الأكسجین، النیتروجین .
- ففي ھذه الحالات التي تنتج جزیئات عالیة القطبیة للغایة ، حیث تحمل ذرة الھیدروجین الصغیرة كمیة لا بأس بھا من الشحنة الموجبة.
- وبما أن النھایة الموجبة لثنائي القطب بإمكانھا الاقتراب عن كثب من النھایة السالبة لثنائي قطب مجاورة ، فقوة التجاذب بین النھایتین كبیرة إلى حد ما. ویدعى ھذا النوع الخاص من التجاذب ثنائي القطب بالرابطة الھیدروجینیة (Hydrogen Bond) وتعادل حوالي % 5 إلى % 10 من قوة الرابطة التساھمیة العادیة .
- والرابطة الھیدروجینیة ھي إحدى أنواع القوى القطبیة (رابطة فیزیائیة) بل أكثر قوة منها ، ومما سبق فإنها تنشا نتيجة فرق كبير في السالبية الكهربية بين ذرة الهيدروجين ( ذي السالبية الكهربية 2.2) في جزئ (المرتبطة أصلاً بذرة أكسجين أو نتيروجين أو فلور) وذرة عنصر آخر مثيل لها سالبية كهربية عالية مثل: (N = 3, O = 3.5, F =4).
- ویتم تكوین ھذه الرابطة من خلال زوج الإلكترون الحر الموجود علي الأكسجين أو الفلور أو النيتروجين التي تنتمي للجزئ الآخر المثيل. وبسبب أن الفرق في السالبیة كبیر فتتكون رابطة قویة .
- ولا یحدث الترابط الھیدروجیني إلا في وجود ذرات الهيدروجين فقط (علل) ، ذلك لأن للذرات الأخرى أغلفة الیكترونیة تحجب أنویتھا عن ذلك الترابط . لهذا نجد أن الرباط الهيدروجيني لا يحدث إلا مع المركبات التي تحتوي على الهيدروجين دون غيرها .
إجابة السؤال
- بالنسبة لسؤالك لم أفهم ما المقصود بالضبط ولكن:
الروابط الهيدروجينة فى جزئ الماء
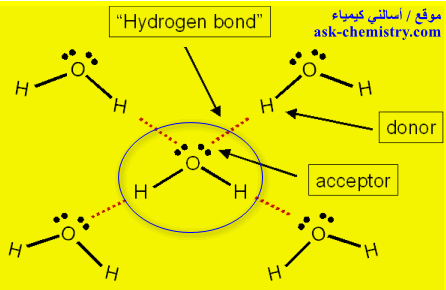
- يتوقف عدد الروابط الهيدروجينية بين الجزئيات على عدد الذرة المستقبلة Acceptors وعدد الذرات المعطية donors في الجزئ.
- في جزئ الماء تتكون شحنة موجبة جزئية Slightly positive charge على كل ذرة الهيدروجين ، وشحنة سالبة جزئية على كل زوج مفرد من الألكترونات على ذرة الأكسجين Slightly negative charge
- حيث يستطيع جزئ الماء تكوين أربع روابط هيدروجينة سوءاً مع جزيئات الميثانول او مع جزيئات أخري من الماء.
- حيث تحتوى ذرة الأكسجين على زوجين من الألكترونات المفردة two lone pairs of electrons قادرين على تكوين عدد (2) من الروابط الهيدروجينية في جزئ ماء آخر.
- وذرتين الهيدروجين فى نفس الجزئ تستطيع تكوين عدد (2) روابط هيدروجينية مع ذرتين من الأكسجين من جزئيات ماء أخري.
- الشكل التالي يوضح كل جزئ ماء وسطى يكون أربع روابط هيدروجينية مع جزئيات الماء الأخري
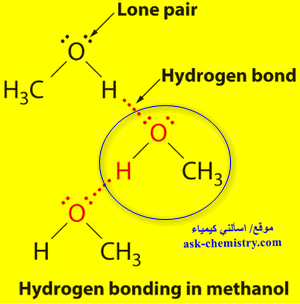
الروابط الهيدروجينة فى جزئ الميثانول R-OH
- بنفس الطريقة السابقة يكون جزي الميثانول الوسطى عدد (2) رابطة هيدروجينية مع جزئيات الميثانول الأخري أو جزئيات الماء المحيطة به.
- حيث تتكون رابطة هيدروجينة بين ذرة الهيدروجين المرتبطة بالأكسجين OH مع أحد الأزواج الحرة من الألكترونات على ذرة أكسجين الجزي الأخر. كما بالشكل التالي:
- السؤال هنا لماذا لم يكون الزوج الحر الآخر الموجود على ذرة الأكسجين رابطة هيدروجينية والإجابة هى لعدم وجود ذرات H كافية مرتبطة بالأكسجين فى المجموعة (OH) لأن كل مركب يحتوى على H واحدة فقط مرتبطة بذرة الأكسجين.
- لذلك فأن جزئ الماء الوسطى يكون 4 روابط هيدروجينية ، وجزئ الميثانول يكون رابطتين هيدروجينيتين.