نصف القطر الأيوني Ionic Radius
- نـصف القطــر الأيوني = هو نصف قطر الأنيون أو الكاتيون.
- طــول الرابطـــة هو مجموع نصفى قطري الأيون الموجب والسالب.
- الأيون عبارة عن ذرة فقدت أو اكتسبت إلكترون أو أكثر لتصل إلى حالة الاستقرار الثماني.
(أ) نصف القطر للأيون السالب
- نصف قطر الايون السالب اكبر من نصف قطر ذرته .
وذلك لان الذرة لتتحول إلى ايون سالب يجب عليها أن تكتسب الكترونات فيزيد عدد الشحنات السالبة في المستويات الرئيسية عن عدد الشحنات الموجبة داخل النواة فتصبح قوة الجذب للنواة موزعة على عدد كبير من الالكترونات فيقل جدب النواة.
(ب) نصف القطر للأيون الموجب
نصف قطر الايون الموجب اصغر من نصف قطر ذرته
لأن الذرة لكي تتحول إلى أيون موجب يجب عليها أن تفقد الكترونات لتصل إلى الاستقرار فيقل عدد الالكترونات في المستويات عن عدد البروتونات في النواة فيزداد قوة جذب النواة للالكترونات
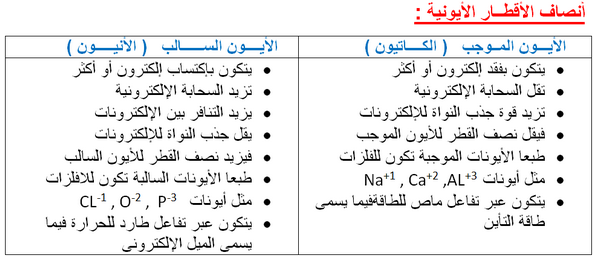
- مقارنة بسيطة بين الأيونات الموجبة والسالبة للتوضيح :
تدرج أنصاف الأقطار الأيونية فى الجدول الدوري
(1) في الدورات
- يوضح الشكل التالي أنصاف اقطار أيونات معظم العناصر الممثلة.
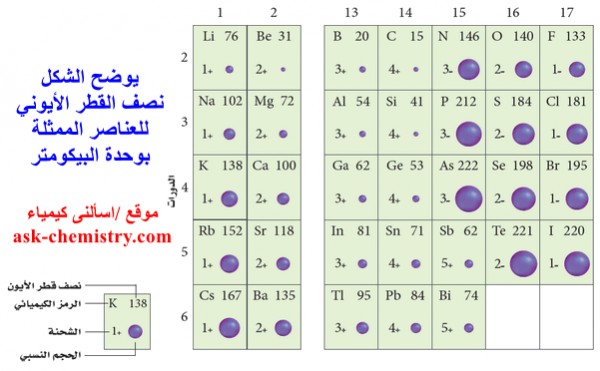
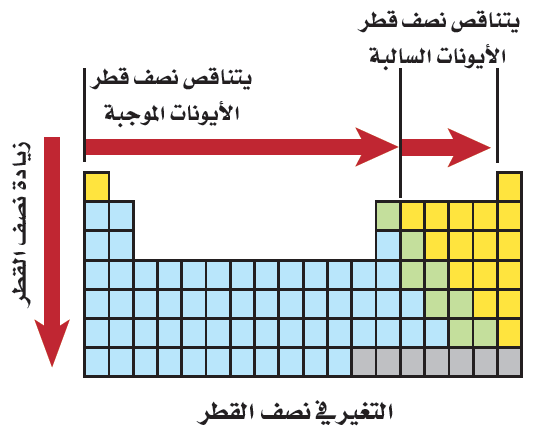
- لاحظ أن العناصر التى فى الجهة اليسرى من الجدول تكون أيونات موجبة أصغر حجماً في حين تكوِّن العناصر التي في الجهة اليمنى من الجدول أيونات سالبة أكبر حجماً.
- وفي الغالب، كلما تحركت من اليسار إلى اليمين عبر الدورة تناقَص حجم الأيون الموجب. وعند بداية المجموعة 15 أو 16 يتناقص حجم الأيون السالب أيضًا تدريجيًّا.
(2) في المجموعات
-عندما تنتقل في المجموعة من أعلى إلى أسفل فإن إلكترونات المستويات الخارجية في الأيون تكون في مستويات طاقة أعلى مما ينتج عنه زيادة فى حجم الأيون، لذا يزداد نصف قطر كل من الأيونات الموجبة والسالبة عند الانتقال إلى أسفل خلال المجموعة.
- يلخص الشكل التالي اتجاه التغير في نصف قطر الأيونات عبر المجموعات والدورات: