طرق تحضير الإلكينات Alkenes
(1) التكسير الحراري للغاز الطبيعي Thermal Cracking of Natural gas
عند تعرض الغاز الطبيعي (البارافينات الغازية) إلى حرارة فوق 600 مo فأن النواتج تكون الإيثيلين والأوليفينات الأحادية الكبيرة.
- يتم الحصول على الأثيلين بهذة الطريقة من خلال سحب الهيدروجين من الإيثان في حرارة تتراوح بين 800 - 820 مo.
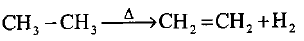
- يمكن زيادة الألكينات المتكونة من خلال استعمال عوامل حفازة مناسبة مثل أكسيد الألمنيوم Al2O3 ، السيلكا SiO2 ، أكسيد الكروم Cr2O3.
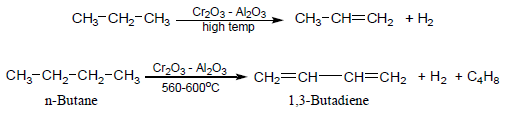
(2) نزع HX من هاليد الألكيل Dehydrohalogenation of alkyl halides
- يحدث تفاعل حذف HX من هاليد الألكيل باستخدام قاعدة قوية في مذيب مناسب مثل الكحول وينتج الألكان المقابل
- يعرف بتفاعل حذف بيتا β-elimination لأنه يتم حذف ذرة الهيدروجين من ذرة الكربون المجاورة لذرة الكربون الحاملة للهاليد.
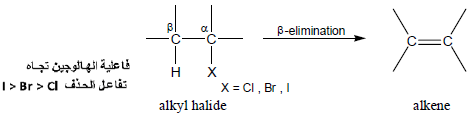
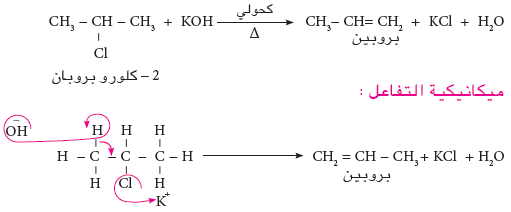
يعتبر هذا التفاعل مفضل لتحضير الألكينات عند استخدام هاليد ألكيل ثالثي يحتوي على هيدروجين بيتا مع قاعدة قوية وذلك لإمكانية التحكم في ناتج هذا التفاعل من خلال حجم القاعدة المستخدمة.
(أ) عند استخدام قاعدة صغيرة الحجم :
فأن المتشكل الأعلى استبدالا (الأعلى ثباتا) يكون هو الناتج السائد ويقال أن ناتج التفاعل في هذه الحالة يتبع قاعدة سيتزف Zaitsev's rule نسبة للكيميائي الروسي سيزيفت Alexander M. Zaitsev الذي لاحظ هذه الظاهرة سنة 1875 م.
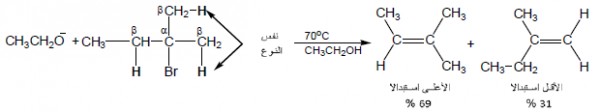
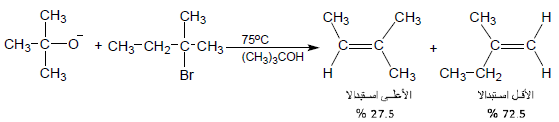
(ب) عند استخدام قاعدة ضخمة الحجم :
يكون الناتج السائد هو الألكين الأقل استبدالا وذلك بسبب الإعاقة المجسامية ويقال أن التفاعل يتبع قاعدة هوفمان Hofmann Rule نسبة للكيميائيى الألماني هوفمان August W. von Hofmann
ملاحظة هامة:
- إن هاليدات الألكيل التي لا تملك هيدروجين بيتا لا تخضع لهذا التفاعل .
- عند استخدام هاليدات ألكيل أولية أو ثانوية فأن التفاعل يعانى من تنافس مع تفاعل الإحلال.
(3) من المركبات ثنائية الهاليد المتجاور Dehalogenation of vicinal halides
تتفاعل الهاليدات الثنائية المتجاورة Vicinal Halides مع مسحوق الخارصين في حمض الخليك أو الكحول الايثيلي أو بمحلول يوديد الصوديوم في الأسيتون ليتكون الألكين:
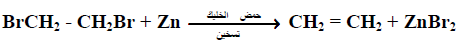
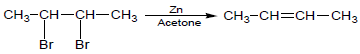
وتعتبر هذه الطريقة محدودة الفائدة كون مثل هذه الهاليدات الثنائية الجوارية عادة ما تحضر من الألكينات ذاتها.
(4) نزع الماء من الكحول Dehydration of alcohols
- يتم ذلك باستعمال عوامل مساعدة مختلفة مثل حمض الكبريتيك المركز فعند مزج الحمض مع الكحول وتسخينهما الى درجة حرارة 165Co يتحرر الاولفين (الاثيلين).
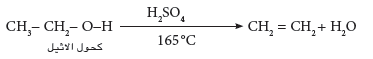
- لابد أن نشير الى أن ذرة الهيدروجين تحذف من على ذرة الكربون المجاورة لذرة الكربون الحاوية على OH.
(5) طريقة كولب Kolb,s method
يتم التحلل الكهربي لمحلول مركز لملح البوتاسيوم أو الصوديوم لحمض مشبع ثنائي الكربوكسيل مثل سكسينات البوتاسيوم ليعطي غاز الإيثين:
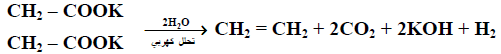
(6) أختزال الألكاينات Reduction of alkynes
- يتم هدرجة الألكاينات فى وجود عامل حفاز مثل البلاتين كالتالي:
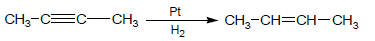
- تحتاج الألكاينات إلى ضعف كمية الهيدروجين التي تحتاجها الألكينات من الهيدروجين بسبب وجود الرابطة الثلاثية في جزيئاتها.
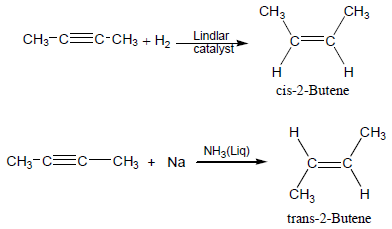
-عند إجراء هدرجة جزئية للألكاينات فإنها تتكون ألكينات Cis أو trans اعتماداً على نوعية العامل الحفاز المستخدم:
فاستخدام الهيدروجين والبلاديوم يكون الناتج Cis- alkene أما استخدام الصوديوم أو الليثيوم في النشادر السائلة ينتج trans-alkene
(7) تفاعل فيتج Witting reaction
تتفاعل أيليدات الفسفور Triphenyle methylidene phosphorane مع مركبات الكربونيل (وخاصة الكيتونات) في درجة حرارة المختبر لإعطاء الألكين المقابل وأكسيد ثلاثي الفوسفين Triphenyl phosphine Oxide
- يمكن تحضير أيليد الفسفور من تفاعل بروميد ثلاثي فينيل مثيل فوسفونيوم مع ليثيوم المثيل.
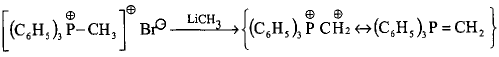
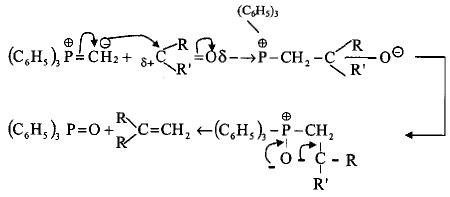
ويتم التفاعل وفق الميكانيكة التالية:
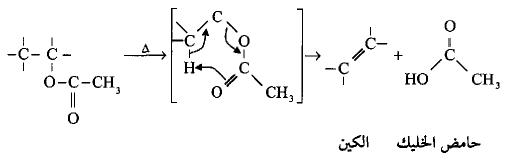
(8) التفكك الحراري للأسيتات Pyrolsis of Acetates
- حين تتعرض الأسيتات (الخلات أو استرات الميثيل) إلى درجات حرارة عالية فأنها تتحلل أو تتفكك من خلال ميكانيكة معينة لتنتج الألكين المقابل وحمض الأستيك (الخليك).
- تتضمن هذة الميكانيكية تشكيل حلقة سداسية (يمكن تصور ذلك باستخدام النماذج المجسمة) حيث تقترب فيها ذرة الأكسجين في مجموعة الكربونيل للأستر من ذرة هيدروجين مجموعة الألكيل في نفس الجزيئة الأمر الذي يساعد في انشطار وتكوين الروابط بشكل متزامن.