الكشف عن كاتيونات المجموعة الثالثة من الشقوق القاعدية
- تشمل هذه المجموعة على أربعة كاتيونات وهي :
1- حديدوز Fe2+) Iron II)
2- حديديك Fe3+) Iron III)
3- الومنيوم Al3+) Aluminium)
4- كروم Cr3+) Chromium)
والتي تترسب على هيئة هيدروكسيدات عند معاملة محاليلها بمحلول هيدروكسيد الأمونيوم NH4OH وفي وجود كمية قليلة من محلول كلوريد الأمونيوم NH4Cl ، وتتميز هيدروكسيدات هذه المجموعة بأنها لا تذوب في الماء.
- كاشف المجموعة : محلول هيدروكسيد الأمونيوم NH4OH وفي وجود كمية قليلة من محلول كلوريد الأمونيوم NH4Cl
- الصورة الترسيبية : هيدروكسيدات ذات ألوان مختلفة وهي كالآتي:
– هيدروكسيد الحديدك (راسب بني) Fe(OH)3
– هيدروكسيد الألمونيوم (راسب أبيض جيلاتيني) Al(OH)3
– هيدروكسيد الكروم (راسب رمادي مخضر) Cr(OH)3
المهم لنا هنا حسب السؤال هو الحديد الثنائي والحديد الثلاثي
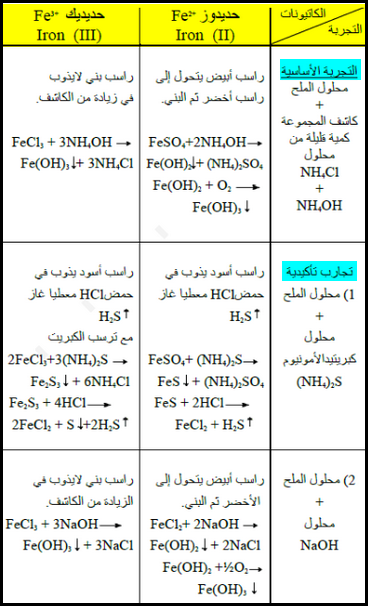
فيما يلي جميع التجارب الأساسية والتأكيدية التى تفرق بين Fe+2 , Fe+3

حل السؤال: لماذاعند تفاعل محلول ثيوسيانات البوتاسيوم مع كلوريد الحديدوز لا يتكون لون ؟
فى التجربة رقم (6) نجد أن كلوريد الحديد (II) لا يعطى لون مع ثيوسيانات البوتاسيوم KSCN وذلك لأن المواد المتقاعلة والمواد الناتجة من التفاعل تكون غير ملونة
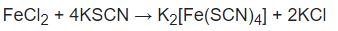
كلوريد الحديدوز غير ملون
ثيوسيانات البوتاسيوم غير ملون
كلوريد البوتاسيوم غير ملون وكذلك tetrathiocyanatoferrate(II) potassium غير ملون