ترتارات الباريوم Barium Tartrate
- مركب كيميائي على هيئة بلورات بيضاء.
- الصيغة الجزيئية له (Ba(C4H4O6
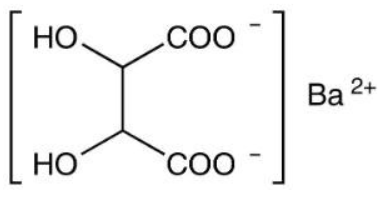
- الكتلة المولية 285.4
- الكثافة = 2.98 جم/سم3
- مركب شحيح الذوبان فى الماء.
- سام ومهيج للعيون والبشرة والرئتين.
- عنصر الباريوم فلز ابيض لين متطاير نسبيا كثافته تبلغ 3.6g/cm3 ، ودرجة انصهاره 850Co ، ودرجة غليانه 1500Co وله وزن نوعي مرتفع.
- اكتشف الباريوم سنة 1774م ، وفي سنة 1800م أعطي له اسم الباريوم وحضر لأول مرة سنة 1808م.
- الباريوم من الفلزات النشطة جدا كالقلويات ويستخدم بكثرة كمادة مزيلة لبقايا الغازات في صمامات الراديو وفي امتصاص الغازات الغير مرغوب فيها.
تجربة تحضير ترتارات الباريوم
(1) تحضر ترتارات الباريوم من تفاعل حمض التارتيك مع كربونات الباريوم حسب التفاعل التالي:
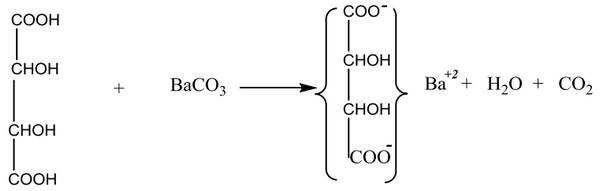
خطوات التجربة:
(1) أذب (2g) من حمض الترتاريك في (10ml) من الماء المقطر.
(2) أضف ببطء مع التحريك (2.5g) من كربونات الباريوم.
(3) سخن مع التحريك المستمر.
(4) حرك المزيج لمدة نصف ساعة للتأكد من تعادل الحمض.
(5) رشح الراسب وأغسله فى الماء البارد ثم جفف عند 100مo