الهاليدات العضوية
- الهاليدات العضوية مركبات تتصل ذرة كربون فيها أو أكثر بذرة هالوجين أو أكثر.
- وقد تكون هاليدات الكيلية عندما تتصل ذرة الهالوجين بمجموعة ألكيلية كما أنها تصنف كهاليدات أروماتية عندما تتصل ذرة الهالوجين بمجموعة أريلية.
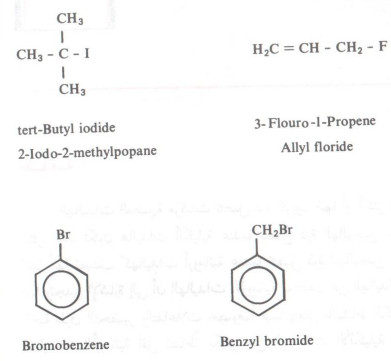
- هذا وتجدر الإشارة إلى أن الهاليدات الأروماتية تختلف عن الهاليدات الألكيلية من ناحية طرق التحضير والتفاعلات خصوصاً فيما يتعلق بالنشاط الكيميائي حيث أن الهاليدات الأروماتية أقل نشاطاً بكثير عن الهاليدات الألكيلية تجاه التفاعلات المختلفة.
الخواص الفيزيائية للهاليدات العضوية
- الصفات الفيزيائية للهاليدات العضوية تتشابه سواء كانت أروماتية أو أليفاتية.
- وبسبب الوزن الجزيئي العالي للهالوجينات تجد أن درجة الغليان لها أعلى من الهيدروكربونات المماثلة لها من ناحية عدد ذرات الكربون.
- كما أن درجة الغليان تزداد بزيادة الوزن الذري للهاليد وذلك في حالة الهاليدات المتماثلة في المجموعة الألكيلية أو الأريلية حيث أن أيوديد الايثل يغلي عند ٧٢مo بينما يغلي بروميد الايثل عند ۳۸مo.
- وبالرغم من أن الهاليدات العضوية تعتبر مركبات قطبية بسبب الفرق في السالبية الكهربائية بين الكربون والهالوجين، إلا أنها لا تذوب في الماء، ربما يعزى ذلك إلى عدم قدرتها على تكوين روابط هيدروجينية مع الماء، إلا أنها تذوب في المذيبات العضوية.

- وتتميز الهاليدات العضوية خاصة التي فيها الهالوجين عبارة عن بروم أو يود أو عديد الكلور بأن لها كثافة أعلى الماء.