الخليط الراسيمي Racemic Mixture
- يشير هذا المصطلح إلى وجود خليط من الإيننتيومرات بنسب متكافئة ويكون غير فعال بصريـاً وذلك لأن تأثير كل إيننتيومر على الضوء المستقطب استوائياً يكون بنفس المقدار ولكن عكس اتجاه الأخــر وبالتالي يلغي النشاط البصري.
- وقد اشتق هذا المصطلح من الكلمة اللاتينية "racemes وتعني عنقود العنب" وتنطق (ray-see-mic) وكان ذلك بعد أن اكتشف الفرنسي Louis Pasteur (157) نوعين من بلورات حمض tartaric في العنب.
- يستخدم أحياناً مصطلح racemate للإشارة إلى أي خليط متكافئ من الإيننتيومرات.
(1) تبلور الخليط الراسيمي Crystallization of Racemic Mixture
- توجد ثلاث أنواع من الخليط الراسيمي وهي مهمة عند فصل بلورات الراسيمات وقـد مـيز بين هذه الأنواع من البلورات الكيميائي الألماني Roozeboom سنة 1899 حيث صنف الراسيمات على أساس الاختلاف في التعبئة الطبيعية للشبكة البلورية crystal lattice
(2) الراسيمات الطبيعية The Nature of Racemates
- عندما تكون الخواص الفيزيائية للبلورة الصلبة غير محددة أو غير معروفة وتحتوي على نسب مولية متكافئة من إيننتيومرات المركب الكيرالي فأنها تعرف بـ racemic modification ويصنف إلى ثلاث أصناف من بلورات الراسيمات.
(أ) التكتل الراسيمي Racemic conglomerate
- أبسط أنواع الراسيمات وهو عبارة عن خليط يدوي أو تكتل لبلورات إيننتيومرين بحيث تتكون الشبكة البلورية من إيننتيومرات متشابهة في اتجاه الكيرالية homochiral كما في الشكل التالي A (كان يعرف بالخليط الراسيمي)
- تكون درجة انصهار التكتل الراسيمي في الغالب أقل من درجة انصهار الإيننتيومر النقي enantiopure وبالتالي عند إضافة كمية قليلةمن أحد الإيننتيومرات إلى الخليط فأن درجة الانصهار تزداد وتكون ذوبانيته أعلى من الإيننتيومر النقي.
(ب) المركب الراسيمي Racemic compound
- يكون في كل وحده بلورية عدد متساو من إيننتيومرات مختلفة في اتجاه الكيرالية (+) ، (-) (أي في نفس البلورة) وهذا يتطابق مع المركب الصلب كما في الشكل التالي B (كان يعرف بالراسيمات).
- يمكن أن تكون درجة انصهار الإيننتيومر النقي أعلى أو أقل من درجة انصهار المركب الراسيمي وعند إضافة كمية قليلة من أحد الإيننتيومرات للمركب الراسيمي فأن درجة الانصهار تقل وذوبانيته أقل من الإيننتيومر النقي ويعرف بالخليط الراسيمي أو الراسيمات.
(جـ) الراسـيمات الكاذبة pseudoracemate
- في هذا النوع تتكون البلورة عشوائياً من الإيننتيومرين وبنسب متكافئة ولكنها غير مرتبة في الطور الصلب وهي حالات نادرة (الشكل التالي C)
- تعرف كذلك بالمحلول الراسيمي الصلب أو البلورات المختلطة mixed crystals وعند إضافة كمية قليلة من أحد الإيننتيومرات للخليط فأن درجة الانصهار لا تتغير مطلقاً أو قد يحدث تغير طفيف لا يذكر.
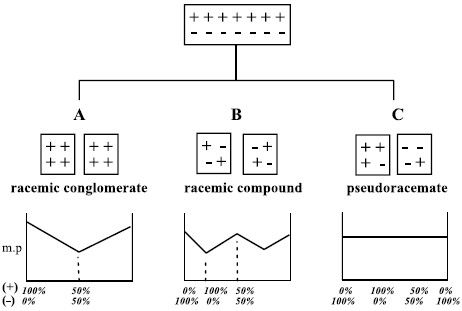
- إن أحد أبسط الطرق للتعرف على نوع الراسيمات هو من خلال مخططات الطور التي تربط التركيب مع درجة الانصهار للحالات الراسيمية الثلاثة التي في الشكل السابق.
- أن أول من أجرى هذا التمييز هو الألماني Roozeboom كتطبيق لقاعدة الطور phase rule.
- النوع الأكثر شيوعاً من أنواع الراسيمات هو المركب الراسيمي B حيث تكون 90% تقريباً من الراسيمات للمواد العضوية الكيرالية على هذه الهيئة وحوالي 10% فقط تكون على هيئة تكتل راسيمي.
- أما النوع الثالث فهو نادراً نسبياً ويكون سلوك هيئة التكتلات أقل شيوعاً من هيئة المركب الراسيمي ولكن بسبب سهولة فصل الإيننتيومرات في حالة التكتل يعطي هذه الفئة أهمية خاصة.
- عندما لا يكون للمركبات الكيرالية نشاط بصري يفترض أنها تتألف بشكل عام من خليط من الإيننتيومرات بنسبة 1:1 بمعنى أنها راسيمات ومع ذلك يجب عدم تجاهل حقيقة أن هذا القياس قد يكون غير أساسي لأن عند اختلاف درجة الحرارة أو الطول الموجي أو استخدام مذيب مختلف يمكن ملاحظة نشــاط بـصــــري وبالتالي تصبح العينة التي نتحدث عنها غير راسـيمية ويقال بأن لها كيرالية خفية cryptochiral
- وليس المقصود بأن الراسيمات التي تعطي مواد كيرالية تكون متواجدة فقط على هيئة بلورة واحده فكثير من الراسيمات تتبلور في كلا الهيئتين (التكتل - والمركب الراسيمي) وذلك اعتماداً على الظروف وعند حدوث هذا تكون أحد الهيئات شبة مستقرة metastable ضمن نطاق معين من الضغط ودرجة الحرارة ففي الحالة الصلبة يمكن للهيئة شبه المستقرة الاحتفاظ ببقائها مده طويلة من دون تغيير.
- عندما تكون هيئتي البلورتين معزولتين يكون هناك فرصه لحدوث تحول داخلي مع أنواع الراسـيمـات الأخرى فعلى سبيل المثال يتبلور 1,1binaphthy1 على هيئة مركب راسيمي له درجة انصهار °154C ويتحول بالتسخين عن طريق الديناميكا الحرارية إلى التكتل الراسيمي الأكثر ثباتاً بدرجة انصهار °159C.
- يطلق على وجود مادة معينة في أكثر من هيئة بلورية اسم متعددة الأشكال polymorphism وهذه الأشكال المتعددة تختلف في درجة الانصهار والتركيب البلوري ويمكن أحياناً أن تتحول من شكل لأخر عن طريق الضغط ودرجة الحرارة والمثال السابق ما هو إلا حالة خاصة من تعدد الأشكال.
- يجب ملاحظة استخدام المصطلحات المناسبة في وصف الحالات فإذا أردنا وصف إيننتيومرين نقيين لمادة كيرالية يستخدم المصطلح enantiomorphous لوصف البلورات الكيرالية في الحالة الصلبة، أما لوصف الجزيئات فيستخدم مصطلح enantiomeric
- وللجزئ يمكن أن يستخدم المصطلحين كيرالي أو غير كيرالي وللعينة الماكروسكوبية الكيرالية يستخدم مصطلح راسيمي وغير راسيمي حيث يدل مصطلح غير راسيمي على أن العينة تتكون بشكل أساسي من جزيئات لها نفس اتجاه الكيرالية homochiral في حين لا يكون مرادف لمصطلح enantiomerically والذي يختصر بـ enantiopure
(3) شبه الراسيمات Quasi-Racemate
- توجد أحياناً مركبات متماثلة في البنية والتوزيع النسبي ولها شكل هندسي متشابه ونفس التصنيف ويمكن أن يحل كل منها محل الأخر في الشبكة البلورية crystal lattice وفي هذه الحالة يطلق عليها اســـــم isomorphous
- فمثلاً إذا كان لدينا مركبين متشابهين ولكن لهما اتجاه كيرالية مختلف heterochiral مثل المركبين chlorosuccinic acid-(+) و bromosuccinic acid-(-) فأنه يطلق عليهمـا أشــبــاه الإيننتيومرات quasi-enantiomers فعند خلطهم بنسب متكافئة من الجزيئات يمكن أن ينتج شبه راسيمي كما في الراسيمي الحقيقي وتكون على هيئة مركب شبه راسيمي أو محلول شبه راسيمي صلب
- من هنا تتضح أهمية أشباه الراسيمات لأنها تربط بين التوزيع المجسم لجزيئات مختلفة.
(4) خليط سكاليمك Scalemic Mixture
- في بعض الحالات تكون نسب خليط من الإيننتيومرات غير متكافئ الجزيئات ويصبح الإيننتيومر الموجود بنسبة أكبر هو السائد في الخليط ويكون هذا الخليط نشط بصرياً لذا يوصف بأنه خليط سكاليمك.
- قد اشتق هذا المصطلح من الكلمة اليونانية scalemos وتعني "غير متوازن".