العناصر المثالية Representative Elements
- انظر إلى العمود الأول من اليسار فى الجدول الدوري تجد أنه يشمل العناصر: Fr ، Cs ، Rb ، K ، Na ، Li ، H ويُسمّى هذا العمود المجموعة 1A.
- باستثناء الهيدروجين تتفاعل جميع عناصر المجموعة 1A بشدّة مع الماء فتصدر فقاعات.

- يُسمّى العمود التالي إلى اليمين المجموعة 2A التي تبدأ بعنصر Be.
- يشار إلى كافة المجموعات من 1A إلى 7A ، والمجموعة 8A (تقع على أقصى يمين الجدول الدوري) بالعناصر المثالية Representative Elements لأنها تظهر مدى واسعاً لكلّ من الخواص الفيزيائية والكيميائية.
- يمكن تقسيم العناصر المثالية إلى ثلاثة أقسام كبيرة: الفلزات - اللافلزات - أشباة الفلزات.
(أ) الفلزات Metals
- باستثناء الهيدروجين، إنّ العناصر المثالية الواقعة إلى اليسار في الجدول الدوري هي فلزات.
- تتميز الفلزات Metals بالتوصيل الكهربائي العالي ، واللمعان ، قابلية السحب لتكوين أسلاك ، وقابلية الطرق (قابلية التطريق لتكوين صفائح رقيقة) .

- تُسمّى عناصر المجموعة 1A (الفلزات القلوية) Alkali Metals ، وتُسمّى عناصر المجموعة 2A (الفلزات القلوية الأرضية) Alkaline Earth Metals.
- تشمل الفلزات أيضاً العناصر الانتقالية Transition Metals ، والعناصر الانتقالية الداخلية Inner Transition Metals.
- تكوّن هذه العناصر معًا عناصر المجموعة B.
- يُعتبر النحاس والفضة والذهب والحديد من العناصر الانتقالية الشائعة.
- يُطلق أيضاً على العناصر الانتقالية الداخلية، والتي تقع تحت الجزء الرئيسيي من الجدول الدوري ، اسم العناصر الأرضية النادرة Rare Earth Elements
- %80 تقريبًا من كل العناصر فلزات صلبة (باستثناء عنصر واحد) في درجة حرارة الغرفة.
- يوضع الشكل التالي وهو عنصر الزئبق السائل الاستثناء الوحيد لهذه القاعدة.
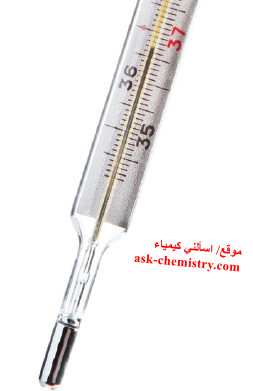
- الزئبق فلزّ انتقالي ، وهو العنصر الفلزّي الوحيد الذي يوجد على هيئة سائل في درجة حرارة الغرفة ، وهو يُستخدم في الترمومترات والبارومترات وكموصل كهربائي (وسيلة اتصال) في الترموستات (مثبّت أتوماتيكي لدرجة الحرارة).
الفلزات الضعيفة
- الفلزات الضعيفة (أو بعد العناصر الإنتقالية) هي فلزات تحت المستوى p.
- تقع بين أشباه الفلزات والفلزات الإنتقالية.
- لها سالبية كهربائية أكبر من الفلزات الإنتقالية الأولى، وأكبر من الفلزات القلوية والفلزات القلوية الأرضية.
- درجات الإنصهار والغليان بصفة عامة أقل من الفلزات الإنتقالية.
- الفلزات الضعيفة أقل صلابة أيضاً.
- الفلزات الضعيفة هي: Al, Ga, Sn, In, Bi, Pb, Tl.
(ب) اللافلزات Non Metals
- تشغل اللافلزات Non Metals الجزء الأيمن العلوي من الجدول الدوري.
- بصفة عامة ، لا تملك اللافلزات لمعاناً مميّزاً كالفلزات ، وهي ضعيفة التوصيل للكهرباء ، كما أنّها هشة في الحالة الصلبة.
- بعض من هذه العناصر، مثل الأكسجين والكلور ، غازات على درجة حرارة الغرفة ، وبعضها، مثل الكبريت فهو صلب وهش.

- الشكل السابق يوضح عنصر الكبريت وهو عنصر لا فلزّي ، درجة انصهاره منخفضة ، ويوجد في حالة صلبة متبلّرة أو في حالة غير متبلّرة . يُستخدم الكبريت أساسًا في صناعة حمض الكبريتيك.
- يوجد عنصر واحد، وهو البروم، سائل أحمر داكن مدخن على درجة حرارة الغرفة.
- هناك مجموعتان جميع عناصرها لافلزات هما الهالوجينات والغازات النبيلة.
الهالوجينات
- هي لا فلزات المجموعة 7A ومن بينها الكلور والبروم.
الغازات النبيلة
- هي لافلزات المجموعة 8A. تُسمّى أحيانًا بالغازات الخاملة، وذلك لقدرتها المحدودة نسبيًّا على التفاعل كيميائياً.
- على سبيل المثال ، يُستخدم النيون في ملء الأنابيب الزجاجية المستخدمة في المصابيح بغرض الإضاءة.
(جـ) أشباه الفلزات Metalloids
- انظر إلى يمين الجدول الدوري الحديث ولاحظ أن الخط العريض المتعرّج على هيئة درجات السلم، والمرسوم بين البورون والأستاتين، يمثل تقريبًا الحدود بين السلوك الفلزي واللافلزي.
- العناصر المجاورة للخط مباشرة لها صفات أشباه الفلزات Metalloids ، وهي تمثل القسم الثالث من العناصر المثالية.
- هذه العناصر لها صفات متوسطة بين تلك الفلزات واللافلزات.
- تُستخدم كمواد شبه موصلة للكهرباء.
- السيليكون والجرمانيوم عنصران مهمان من عناصر أشباه الفلزات ، ويُستخدمان في تصنيع الشرائح الرقيقة لأجهزة الكمبيوتر والخلايا الشمسية.
- يصعب عليك تعلّم الخواص الكيميائية والفيزيائية لأكثر من 100 عنصر وتذكرها من دون الاستعانة بالجدول الدوري.
- عوضا عن حفظ خواصها كل على حدة ، عليك فقط تعلم السلوك العام والاتجاه (الميل) داخل المجموعات الخاصة. وبالتالي، تكتسب معلومات فعالة ومفيدة عن خواص معظم العناصر.