إلكترونات التكافؤ Valence Electrons
- تساعدك معرفة الترتيبات الإلكترونية لكلّ من الصوديوم والكلور على فهم سبب اتحاد هذه الذرّات مع بعضها لتكوين كلوريد الصوديوم.

- تشرح الترتيبات الإلكترونية سبب كتابة وحدة الصيغة لكلوريد الصوديوم بالصيغة NaCl وليس Na2Cl أو NaCl2.
- يمكن التوصل إلى الإجابة عن الأسئلة المتعلقة بخواص الكثير من المركبات عبر معرفة ترتيبها الإلكتروني، والإجابة عن أسئلة أخرى مثل لماذا يوصل كلوريد الصوديوم المنصهر الكهرباء؟ ولماذا نقول إنّ كلوريد الصوديوم هو مادة صلبة ذات درجة انصهار مرتفعة؟
- لعلك تتذكر أن مندليف قد استخدم أوجه التشابه في خواص العناصر لترتيب جدوله الدوري.
- واكتشف العلماء بعد ذلك أن خواص العناصر الموجودة في كل مجموعة من مجموعات الجدول الدوري متشابهة، نظرًا لأن لها العدد نفسه من إلكترونات التكافؤ.
- إلكترونات التكافؤ Valence Electrons هي الإلكترونات الموجودة في أعلى مستوى طاقة مشغول في ذرّات العنصر.
- يحدّد عدد إلكترونات التكافؤ بشكل كبير الخواص الكيميائية لعنصر ما، ومن إحدى طرق تعيين هذا العدد هي فحص الترتيب الإلكتروني للعنصر .
إلكترونات التكافؤ بحسب المجموعة
- يرتبط عدد إلكترونات التكافؤ أيضًا بأرقام المجموعات في الجدول الدوري.
- لإيجاد عدد إلكترونات التكافؤ لعنصر ممثل ما ، يكفي النظر إلى رقم المجموعة التي يوجد فيها.
- على سبيل المثال، تحتوي عناصر المجموعة 1A كلها (الهيدروجين، الليثيوم، الصوديوم، البوتاسيوم ... إلخ) على إلكترون واحد وهو ما يتوافق مع رقم 1 في المجموعة 1A.
- يحتوي كل من الكربون والسيليكون في المجموعة 4A على أربعة إلكترونات تكافؤ.
- يوضح الشكل التالي تطبيقات عناصر هذه المجموعة وبعض استخداماتها.
- يُستخدم الماس ، وهو شكل من أشكال الكربون ، في صناعة المجوهرات.
- أما السيليكون ، فيستخدم لصنع الرقائق الإلكترونية.

- يحتوي كل من النيتروجين والفوسفور في المجموعة 5A على خمسة إلكترونات تكافؤ ، فيما يحتوي كل من الأكسجين والكبريت في المجموعة 6A على ستة إلكترونات تكافؤ .
- الغازات النبيلة هي الاستثناء الوحيد لهذه القاعدة، فالهيليوم له إلكترونا تكافؤ اثنان فقط فيما جميع الغازات النبيلة الأخرى لها ثمانية إلكترونات تكافؤ.
الترتيبات الإلكترونية النقطية Electron Dot Structure
- تعتبر إلكترونات التكافؤ الإلكترونات الوحيدة التي تستخدم عادة في تكوين الروابط الكيميائية، ولذلك فهي كقاعدة عامة، الإلكترونات الوحيدة التي تظهر في الترتيبات الإلكترونية النقطية.
- الترتيبات الإلكترونية النقطية Electron Dot Structures هي الأشكال التي توضح إلكترونات التكافؤ في صورة نقاط.
- يوضح الجدول التالي الترتيبات الإلكترونية النقطية لذرّات بعض عناصر المجموعات A.
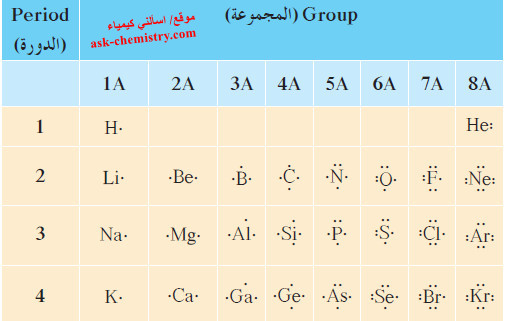
- لاحظ في الجدول أن جميع عناصر المجموعة الواحدة (باستثناء الهيليوم) لها عدد النقاط الإلكترونية نفسه في الترتيب الخاص بكل عنصر.