السالبية الكهربية Electronegativity
- السالبية الكهربية هي قدرة الذرة على جذب إلكترونات الرابطة الكيميائية.
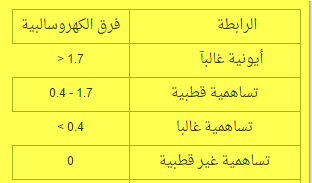
- يتم تحديد نوع الروابط الكيميائية بين الذرات حسب الفرق في السالبية الكهربية بين الذرات كما هو موضح بالجدول :
تدرج السالبية الكهربية فى الجدول الدورى
1- فى الدورات الأفقية:-
تزداد السالبية الكهربية إذا اتجهنا من اليسار إلى اليمين أى بزيادة العدد الذرى ونقص نصف القطر وهذا يؤدى إلى زيادة قوة جذب النواة لإلكترونات الرابطة.
2- فى المجموعات الرأسية:-
تقل السالبية الكهربية من أعلى إلى أسفل أى بزيادة العدد الذرى وزيادة نصف القطر وهذا يؤدى إلى نقص قوة جذب النواة لإلكترونات الرابطة.
ملاحظات هامة
1- الفلور يعتبر أكبر العناصر سالبية كهربية.
2- الفرق فى السالبية الكهربية للعناصر له دور فى تحديد نوع الرابطة بين الذرات.
3- الفلزات لها أقل سالبية لكبر نصف قطرها.
4- اللافلزات لها أكبر سالبية لصغر نصف قطرها.
5- تعتمد السالبية الكهربية على الحجم الذري فالذرة الأصغر حجماً تكون الأعلى فى السالبية الكهربية .
6- العناصر ذات السالبية الكهربائية الأعلى في الجدول الدوري هي النيتروجين و الأكسجين و الهالوجينات (عناصر المجموعة 17).
7- العناصر ذات السالبية الكهربائية الأقل في الجدول الدوري هي الفلزات القلوية ( مجموعة 1 ) و الفلزات القلوية الأرضية (مجموعة 2 ).
8- الغازات النبيلة بعضها لا يمكن تعيين السالبية الكهربائية له لأنه لا يكون مركبات،وعندما يكون الغاز النبيل مركبات تكون سالبيته الكهربائية عالية جداً و مشابهة لقيمة السالبية الكهربائية للهالوجينات.
السالبية الكهربية فى المركبات العضوية
- المجموعات المعطية للألكترونات تقلل من السالبية الكهربية فى المركب
- المجموعات الساحبة للألكترونات تزود من السالبية الكهربية في المركب