الأكسدة Oxidation
هي عملية فقد إلكترونات ينتج عنها زيادة فى الشحنة الموجبة.

- أو ھي الزيادة في عدد الأكسدة.
- العامل المؤكسد ھو المادة التي تؤكسد مادة أخرى تتفاعل معھا ، وتحدث لھا عملية اختزال (تكتسب إلكترونا أو أكثر)
عدد التأكسد ( رقم الأكسدة) Oxidation number
- هو عدد الإلكترونات التى يمكن أن يفقدها أو تكتسبها أو تساهم بها ذرة العنصر خلال التفاعل .
- وفي المركبات التساهمية يُعرف عدد الأكسدة على أنه الشحنة التى تحملها الذرة لو حددنا إلكترونات الروابط التساهمية للذرة الأكثر سالبية كهربائية.
قواعد تحديد أعداد الأكسدة للعناصر :
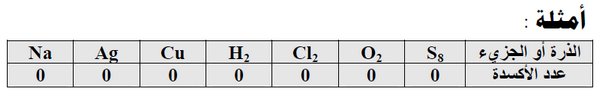
(1) عدد الأكسدة للعنصر النقي (الحر) غير المرتبط بغيره (ذرة أو جزئ) يساوي صفراً.
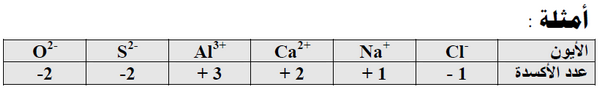
(2) عدد الأكسدة للايونات أحادية الذرة يساوي شحنتها.
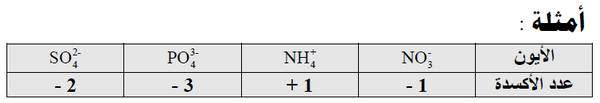
(3) مجموع أعداد الأكسدة لجميع الذرات في ايون يجب أن تساوي الشحنة الموجودة على ذلك الأيون.
(4) مجموع أعداد الأكسدة لجميع الذرات فى مركب متعادل (لا يحمل شحنة) يساوي صفراً.

(5) عدد الأكسدة للهيدروجين في جميع مركباته هو (+1) باستثناء هيدريدات الفلزات مثل هيدريد الصوديوم (NaH) وهيدريد الكالسيوم (CaH2) فإن عدد الأكسدة له (-1).
(6) عدد الأكسدة للأكسجين فى جميع مركياته (-2) ماعدا :-
أ- مركبات فوق الأكسيد مثل فوق أكسيد الهيدروجين (H2O2) وفوق أكسيد الصوديوم (Na2O2) وفوق أكسيد البوتاسيوم (K2O2) وفوق أكسيد الكالسيوم (CaO2) فأن عدد الأكسدة للأكسجين فيها يساوي (-1).
ب- مركب فلوريد الأكسجين (OF2) عدد الأكسدة للأكسجين فيه هو (+2) لأن السالبية الكهربائية للفلور أعلى من الأكسجين.
جـ - مركب سوبر أكسيد البوتاسيوم (KO2) عدد الأكسدة للأكسجين فية هو (1/2-) .
(7) عدد الأكسدة لعناصر المجموعة الفلزية (1A) (الفلزات القوية ) في مركباته تساوي (+1). ومن أمثلة الفلزات القلوية : (Rb-K-Na-Li)
(8) عدد الأكسدة لعناصر المجموعة السابعة ( الهالوجينات) غالباً تساوي (-1) ومن أمثلة الهالوجينات : (F-Cl-Br-I). أما إذا ارتبط الهالوجين بذرات ذات سالبية كهربية أعلى منه مثل الأكسجين فإن عدد أكسدة الهالوجين سوف يأخذ عدد أكسدة موجب
مثل :
Cl2O عدد أكسدة الكلور = +1 ، HClO3 عدد أكسدة الكلور = +5