تأثير الأزاحة الألكترونية
- هو التأثير الناتج عن أزاحة الألكترونات فى المركبات العضوية.
- ويسمى بالأنجليزية : Electron Displacement Effects أو electron delocalisation effect
- يتم تصنيف هذا التأثير كالتالي :
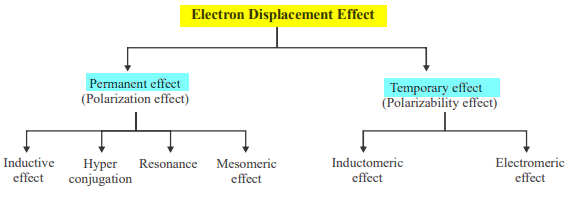
التأثير الحثي Inductive effect
- التأثير الحثي هو أزاحة دائمة لزوج الألكترونات المشاركة فى تكوين الرابطة في اتجاه الذرة أو المجموعة الأكثر سالبية كهربية.
- التأثير الحثي هو قطبية مستحثة تنشأ في الرابطة التساهمية بسبب الاختلاف في السالبية الكهربية بين الذرات المتصلة ببعض.
- التأثير الحثي في الكيمياء والفيزياء هو تأثير يلاحظ تجريبياً وهو ناتج من انتقال الشحنة عبر سلسلة من الذرات في جزئ ما بواسطة الحث الكهربي. والتأثير القطبي الكلي المبذول بواسطة مستَبْدَل عبارة عن مزيج من التأثير الحثي والتأثير الميزوميري.
التاثير الحثي السالب والموجب (I , +I-)
- السحابة الإلكترونية في الرابطة سيجما σ-bond التي تربط بين ذرتين مختلفتين ليست متماثلة على جانبي الرابطة ولكنها مزاحة قليلاً باتجاه الذرة الأكثر سالبية كهربية. وهذا يسبب حالة ثابتة من القطبية للرابطة حيث تحمل الذرة الأكثر سالبية كهربية شحنة سالبة جزيئية (δ-) بينما تحمل الذرة الأخرى على شحنة موجبة جزيئية (δ+).
- إذا اتصلت الذرة الأكثر سالبية بسلسلة من الذرات (عادة سلسلة كربونية) فإن الشحنة الموجبة تُرَحَّل إلى الذرات الأخرى في هذه السلسلة، وهذا هو التأثير الحثي الساحب للإلكترونات electron-withdrawing ويرمز إليه بـ (I-) أي التأثير الحثي السالب.
- بعض المجموعات، مثل مجموعات الألكيل تكون أقل من الهيدروجين في سحب الإلكترونات ولهذا تعتبر مجموعات طاردة للإلكترونات electron-releasing وبالتالي يكون لها تأثير حثي موجب ويرمز إليه بـ (I+).
- كلما كانت القطبية المستحثة أقل من القطبية الأصلية، كان التأثير الحثي أسرع اختفاءً ومؤثراً فقط على مسافة قصيرة.
- التأثير الحثي تأثير دائم ولكنه ضعيف لأنه يتضمن إزاحة إلكترونات الرابطة القوية سيجما، بالإضافة إلى عوامل أخرى أقوى من ممكن أن تحجبه.
أهمية التأثير الحثي
- التأثير الحثي يمكن استخدامه لتحديد ما إذا كان الجزيء مستقر أم لا أعتماداً على الشحنة التي تحملها الذرة المعتبرة ونوع المجموعات المتصلة بها.
(1) إذا كانت هناك ذرة تحمل شحنة موجبة ومتصلة بمجموعة لها تأثير حثي سالب سوف تتضخم شحنتها الموجبة وبالتالي سوف يصبح الجزيء أقل استقراراً (مما إذا لم يؤخذ هذا التأثير في الاعتبار) من الحالة التي لا يؤخذ هذا التأثير في الاعتبار.
(2) إذا كانت هناك ذرة تحمل شحنة سالبة ومتصلة بمجموعة لها تأثير حثي موجب فسوف تتضخم شحنتها السالبة مما يجعل الجزيء أقل استقراراً من الحالة التي لا يؤخذ هذا التأثير في الاعتبار.
(3) إذا كانت هناك ذرة تحمل شحنة سالبة ومتصلة بمجموعة لها تأثير حثي سالب سوف تتضاءل شحنتها السالبة مما يجعل الجزيء أكثر استقراراً من الحالة التي لا يؤخذ هذا التأثير في الاعتبار.
(4) إذا كانت هناك ذرة تحمل شحنة موجبة ومتصلة بمجموعة لها تأثير حثي موجب فسوف تتضاءل شحنتها مما يجعل الجزيء أكثر استقراراً من الحالة التي لا يؤخذ هذا التأثير في الاعتبار.
الخلاصة: كلما كانت الذرة تحمل شحنة زائدة كلما كان الجزيء أقل استقراراً والعكس صحيح.
التأثير الميزوميري Mesomeric effect
- كان الكيميائي كريستوفر كيلك إنغولد أول من طرح مبدأ التأثير الميزوميري وذلك سنة 1938 بديلاً عن مبدأ الرنين المرادف الذي طرحه لينوس باولنغ.
- هو القطبية الناتجة فى الجزي بواسطة التأثير المتبادل بين رابطتين من النوع (π) أو بين رابطة من النوع (π) وزوج مفرد من الألكترونات الموجود على ذرة مجاورة.
- يحدث بكثرة فى حالات الروابط الثانئية (double bond) حيث يتضمن عدم تمركز ألكترونات الرابطة (π)
- هو خاصية توجد لدى المستبدلات أو المجموعات الوظيفية في المركبات الكيميائية يمكن بموجبها إجراء توصيف نوعي لمدى مقدرة سحب الإلكترونات أو مانحة للإلكترونات اعتماداً على التركيبات الرنينية الموافقة conjugated structures
- يرمز لهذه الخاصية بالحرف M
التاثير الميزوميري السالب والموجب (M , +M-)
- يكون التأثير الميزوميري إيجابي (+M) عندما يكون المستبدل مانحاً للإلكترونات.
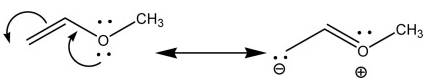
- في حين أن التأثير السلبي (–M) يكون للمجموعات الساحبة للإلكترونات.
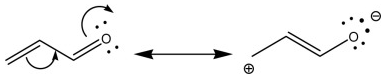
- الجدول التالي يوضح المستبدلات ذات التأثير الأيجابي أو السلبي
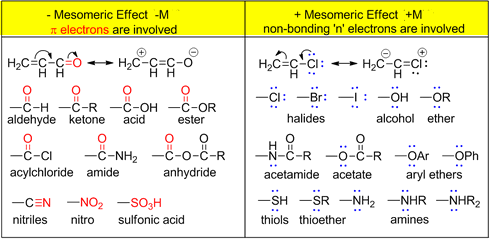
- ترتيب المستبدلات ذات التأثير الميزوميري الإيجابي (+M)
O− > –NH2 > –NHR > –OR > –NHCOR > –OCOR > –Ph > –F > –Cl > –Br > –I–
- ترتيب المستبدلات ذات التأثير الميزوميري السلبي (-M)
−NO2 > –CN > -SO3H > –CHO > –C=O > –COOCOR > –COOR > COOH > –CONH2 > –COO–