رسم تركيب لويس لثاني أكسيد الكلور ClO2 Chlorine Dioxide
- لمراجعة خطوات رسم تركيب لويس لأى جزئ يمكن الرجوع إلى هذا الرابط: قواعد رسم تراكيب لويس
(1) يتكون جزئ ثاني أكسيد الكلور ClO2 من ذرة كلور وذرتي أكسجين، ولأن الكلور أقل قوة جذب للإلكترونات المشتركة تصبح ذرة الكلور هي الذرة المركزية، وذرتين الأكسجين هي الذرات الجانبية.
(2) يجب أن نجد العدد الأجمالي لألكترونات التكافؤ المتوافرة للترابط:

هناك 19 إلكترون تكافؤ موجودة للترابط.
(3) حدد عدد أزواج الترابط الكلي . وللقيام بذلك نقسم عدد الإلكترونات المتوافرة على (2)
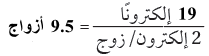
يتوافر 9.5 أزواج من الإلكترونات للترابط. (أى 9 ازواج والكترون واحد مفرد)
(4) ضع زوجًا رابطًا (رابطة أحادية) بين ذرة الكلور المركزية وذرتي الأكسجين الجانبيتين.
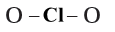
(5) حدد عدد الأزواج غير المرتبطة المتبقية.
اطرح عدد الأزواج المستخدمة في هذه الروابط من العدد الإجمالي للألكترونات المتوافرة للترابط
9.5 أزواج (المجموع الكلي) – 2 أزواج مستخدمة = 7.5 أزواج غير رابطة
(6) أضف ثلاث أزواج غير مرتبطة إلى كل ذرة أكسجين جانبية
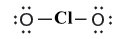
(7) اطرح الأزواج غير المرتبطة من الأزواج المتوافرة المتبقية.
7.5 أزواج (المجموع الكلي) – 6 أزواج مستخدمة = 1.5 أزواج غير رابطة
ولحصول ذرة الأكسجين على ثمانية إلكترونات، يجب أن يكوِّن الجزيء روابط ثنائية.
تفحص التركيب غير المكتمل، وبين مواقع الأزواج غير الرابطة. لاحظ أن ذرة الكلور ليس لها ثمانية إلكترونات ويوجد 1.5 زوج غير رابط أى ثلاث ألكترونات لذلك تضاف إلى ذرة الكلور.
(8) استخدم زوجًا غير مرتبط من كل ذرة أكسجين لتكوين رابطة ثنائية مع ذرة الكلور وأضف الثلاث الألكترونات المتبقية للكلور.

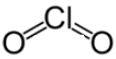
أثبات تركيب لويس لجزئ ClO2
- يتم إثبات تركيب لويس السابق عن طريق حساب الشحنة التقديرية لكل ذرة من الذرات الموجودة فى الجزئ وأن كان مساوية للصفر فالتركيب المموجود صحيح.
- يمكن حساب الشحنة التقديرية من القوانين التالية (وكلها واحد):
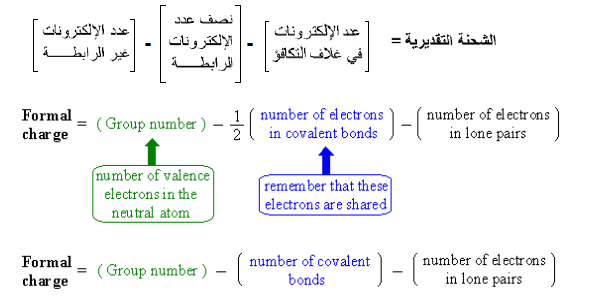
من تركيب لويس السابق لجزئ ClO2 يتم حساب الشحنة التقديرية كالتالي:
- يتم حساب الشحنة التقديرية على ذرة الكلور كما يلي :-
عدد إلكترونات التكافؤ = 7 ، وعدد الإلكترونات الرابطة = 8 ، وعدد الإلكترونات غير الرابطة = 3
formal charge = 7 - 8/2 - 3 = 0
- حساب الشحنة على لكل ذرة الأكسجين :-
عدد إلكترونات التكافؤ = 6 ، وعدد إلكترونات الرابطة = 4 ، وعدد الإلكترونات غير الرابطة = 4
formal charge = 6 - 4/2 - 4 = 0
اذاً الجزئ متعادل لذا فأن تركيب لويس المكتوب أعلاه صحيح
