حساب التركيز بـ ppm
- ppm : وحدة قياس للتركيز وتعنى جزء لكل مليون جزء أى part per million
- ppm : يمكن استخدامها فى حالة التركيز W/V أو W/W أو V/V
- ppm : تعنى جزء واحد من المذاب لكل مليون جزء من المحلول.
- يستخدمها الكيميائيون والفيزيائيون للتعبير عن نسبة تركيز مادة في مادة أخرى.
أسباب إستخدام وحدة ppm
- يستعمل للتعبير عن نسب صغيرة جداً من مادة في مادة أخرى.
- على سبيل المثال : نفترض 1 م3 من الماء وهو يتكون من 1 مليون سم3 من الماء (100 سم في 100 سم في 100سم = 1.000.000 سم3)، وأذبنا فيه 1 سم3 من الملح، فاننا نقول أن الماء يحتوي على ملح بنسبة 1 في المليون (ppm 1).
قوانين ppm
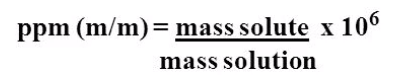
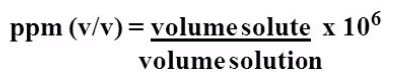
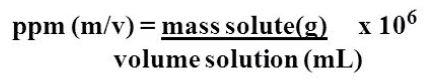
- لاحظ هنا كلمة المحلول تعنى (المذيب + المذاب)
- هناك قوانين أخري يمكن اشتقاقها من القوانين السابقة مثل:



لماذا يتم الضرب فى 106 في القانون التالي:
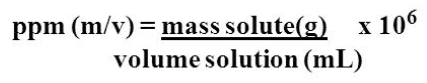
- وذلك بسبب تعريف ppm فهو النسبة بين كتلة جزء واحد من المذاب إلى كتلة مليون جزء من المحلول.
- ولتكبير القيمة وجعلها مختلفة عن الصيغ التعبيرية الأخري للتركيز مثل W/W , W/V , V/V.
- ملحوظة هامة : القانون الأكثر أستخداماً فى القياسات الدولية هو ppm = mg/L