أولأ: مركبات العناصر الانتقالية ملونة
- يرجع ذلك لوجود إلكترونات مفردة في أوربتالات المستوى الفرعي (d).
- الطاقة اللازمة لإثارة هذة الألكترونات المفردة تساوى طاقة الضوء المرئي فتمتص جزء منه اللازم للإثارة وتظهر باللون المتمم.
ثانياً/ متى يكون المركب عديم اللون
يكون المركب عديم اللون فى ثلاث حالات وهي:
(1) عندما يكون المستوى الفرعي (d) تام الامتلاء أى أن جميع الإلكترونات في حالة إزدواج.
(2) لا توجد إلكترونات فى المستوى الفرعي (d) أى يكون فارغاً.
(3) وجود الإلكترونات فى المستوى الفرعي (s) او (p) وهي تحتاج لإثرتها إلى طاقة أعلى من طاقة الضوء المرئي.
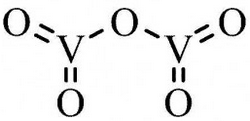
ثالثاً/ خامس أكسيد الفانديوم Vanadium pentoxide
- مركب كيميائي له الصيغة الكيميائية V2O5
- يوجد على شكل بلورات صفراء اللون. (أى أنه ملون)

- له دور هام ايضاً في الاصباغ التي تدخل في صناعة السيراميك و الزجاج حيث يعمل كمرسخ للون (أى مثبت للألوان أو الأصباغ)
- عدد تأكسد الفانديوم (عدده الذري 23) فى هذا المركب هو +5 ويكون التوزيع الإلكتروني له كالتالي:
V+5 : [Ar]18 , 4s0 3d0
ومن التوزيع الإلكتروني السابق نجد أن المستوى الفرعي (3d) فارغ ولا يحتوى على إلكترونات مفردة لذلك من المتوقع أن يكون غير ملون حسب القواعد السابقة ولكن هذا لا يحدث فمركب خامس أكسيد الفانديوم مركب ذو بلورات صفراء اللون... ولكن ما السبب؟ وما هذا الشذوذ عن القاعدة؟
رابعاً/ نظرية المجال البلوري
- تنقسم المستوى الفرعي (d) إلى خمس مدارات غير متمائلة وهي:
(1) مدارات t2g والتى توجه فيها فصوص المدار(d) بين المحاور (x , y , z) وهي dx-y , dx-z , dy-z
(2) مدارات eg وفيها توجة الفصوص على طول المحاور وهي dx2-y2 , dz2
- أستطاعت نظرية ال المجال البلوري وضع تفسير مقنع وواضح لظهور الألوان في متراكبات الفلزات الانتقالية وأرجعت ذلك إلا أن الألكترون المفرد ينتقل من المجموعة (t2g) إلى المجموعة (eg) ثم يعود وعند عودته يطلق موجة فى المجال المرئي، فتمتص جزء منه اللازم للإثارة وتظهر باللون المتمم.
- وعلى ذلك فأن نظرية المجال البلوري تهدف إلى انتقال الألكترون المفرد داخل أوربتالات (d) والفانديوم (+5) لا يحتوى على إلكترونات أصلاً فى أوربتال (d) لذلك فهي لم تستطع تفسير اللون فى خامس أكسيد الفانديوم.
خامساً/ تفسير اللون فى خامس أكسيد الفانديوم
- يرجع ظهور اللون فى خامس أكسيد الفانديوم نتيجة انتقال الإلكترونات من الليجاند (O2- هنا) إلى ذرة الفلز المركزي وذلك حسب نظرية (ligand-metal charge transfer (LMCT ( نظرية معقد انتقال الشحنة).
- معقد انتقال الشحنة هو معقد تناسقي يعتمد في تركيبه على وجود جزيء مانح (مثل O2 هنا) وآخر مستقبل للإلكترونات (مثل الفانديوم هنا)؛ حيث يؤدي التجاذب الكهربائي الساكن إلى استقرار المعقد.
- إن طبيعة التجاذب بين هاتين الوحدتين لا يصنف ضمن الترابط الكيميائي، والكثير منها تخضع لانتقالات إلكترونية جزيئية للوصول إلى حالة مثارة بحيث يحدث امتصاص للضوء نتيجة انتقال جزء من الشحنة الكهربائية بين الوحدتين المكونتين للمعقد؛ ولذلك فإن لتلك المعقدات ألوان شديدة؛ مثلما هو الحال مع معقد الأكسجين مع الفانديوم الذي له لون بلورات صلبة صفراء.