أكتب أعداد الكم الأربعة للإلكترون السابع في ذرة الأكسجين؟
- نكتب التوزيع الألكتروني لذرة الأكسجين
O8 : 1s2 , 2s2 2p4

لذلك يكون:
عدد الكم الرئيسي: n = 2 لأن الترتيب الإلكتروني انتهى بالمستوى الرئيسي الثاني
عدد الكم الثانوي: l = 1 لأن الترتيب الإلكتروني انتهى بالمستوى الفرعي (p)
عدد الكم المغناطيسي: ml =0 لأن الألكترون السابع يقع فى الاوربتال (2py) الذي قيمة ml = 0
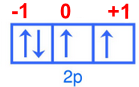
عدد الكم المغزلي: ms = +1/2 لأن الإلكترون السابع هو إلكترون مفرد فى الأوربتال 2py
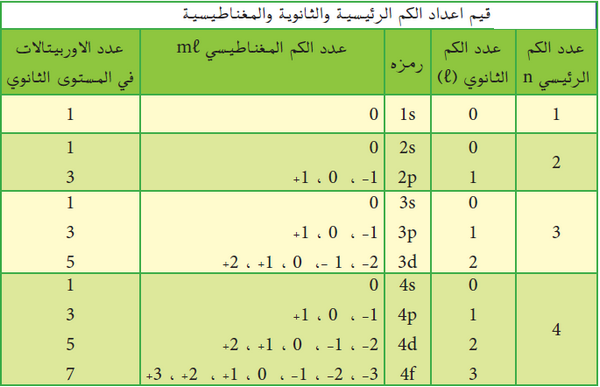
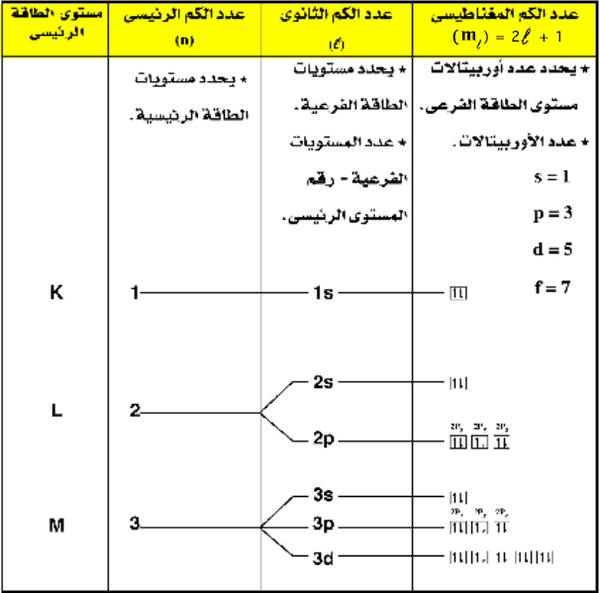
تلخيص أعداد الكم للإلكترونات حتى مستوى الطاقة الرابع
مصادر مهمة عن أعداد الكم
(1) كتاب مقدمة فى التركيب الألكتروني للذرة والكيمياء النووية أعداد الكم ص51
(2) كتاب المفاهيم الأساسية للكيمياء العامة أعداد الكم ص221
(3) كتاب أساسيات الكيمياء الفيزيائية كيف وجد شرودنجر أعداد الكم الثلاثة ص34
(4) شرح مفصل عن أعداد الكم