عناصر مجموعة النيتروجين 5A
- تقع عناصر مجموعة النيتروجين في المجموعة (5A) وتضم: النيتروجين - الفوسفور - الزرنيخ - الأنتيمون - البزموث.
- لكل عنصر من عناصر المجموعة 5A خمسة إلكترونات تكافؤ وتوزيع إلكتروني ينتهي بـ ns2 np3
- النيتروجين ضعيف النفاذية المغناطيسية ، مما يعني أنه لا ينجذب إلى المجال المغناطيسي ، وهذا يدل على أنه إلكتروناته جميعها مرتبطة.
- للنيتروجين عدد تأكسد يتراوح بين 3- و 5+
- للفوسفور والزرنيخ والأنتيمون أعداد تأكسد 3- و 3+ و 5+
- للبيزموث أعداد تأكسد 3+ و 5+
- تقل طاقات التأين الأولى والكهروسالبية ، ويزداد نصف القطر الذري كلما انتقلنا إلى أسفل المجموعة.
الخاصية الفلزية واللافلزية لعناصر المجموعة 5A
- نجد أن عناصر هذة المجموعة تختلف فى خاصيتها الفلزية واللافلزية حيث يلاحظ أن النيتروجين والفوسفور عناصر لافلزية.
- ثم تندرج هذة الخاصية فنجد أن الزرنيخ والأنتيمون أشباة فلزات ولكن هذين العنصرين يسلك كل منهما سلوكاً مختلفاً حيث نجد أن الزرنيخ يسلك سلك اللافلزات بينما الأنتيمون يسلك مسلك الفلزات.
- العنصر الأخير فى هذة المجموعة وهو عنصر البزموث له خواص فلزية واضحة.
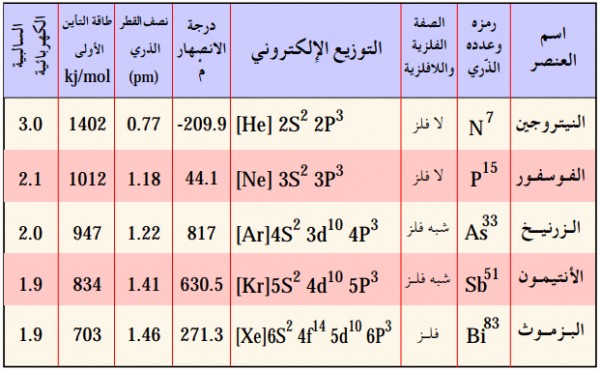
- الجدول التالي يوضح أهم الخصائص لعناصر مجمجموعة النيتروجين 5A
اختبار اللهب لعناصر المجموعة 5A
- ظهور اللهب هى ظاهرة مميزة لكل عنصر مثل بصمة الأصابع للإنسان.
- عندما يوضع العنصر على النار يكتسب طاقة فتنتقل الألكترونات من مستوى طاقة أقل إلى مستوى طاقة أعلى (إثارة) ولأن هذا يجعل العنصر غير مستقر فأنه يعاود الرجوع إلى مستوى طاقته الأصلى وتنطلق طاقة على هيئة ضوء.
- العناصر اللافلزية لا يمكن تمييزها بواسطة كاشف اللهب لأن قابليتها للإثارة ضعيف جداً.
- لا يمكن تعرُّف عناصر المجموعة 5A من خلال اختبارات اللهب؛ لأن معظم هذه العناصر لافلزية وترتبط بغيرها من خلال الروابط التساهمية، ماعدا:
الأنتيمون الذي يصدر ضوءًا أخضر خافتًا أو أزرق عند تعريضه للهب.
والبزموث الذي يصدر ضوءًا أزرق مائلاً إلى البنفسجي.