أولاً/ درجة الغليان فى الألكانات
- تزداد درجة الغليان تزايد منتظم بزيادة الوزن الجزيئي بغض النظر عن التركيب البنائي للجزئ.
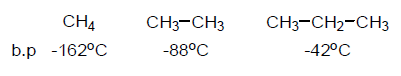
- عند التساوي في الوزن الجزيئي فأن درجة الغليان تعتمد على التركيب البنائي للجزئ كما يلي :-
(أ) تقل درجة الغليان بزيادة التفرع على السلسلة حيث تعمل هذه التفرعات على إبعاد الجزئيات عن بعضها فتقل بذلك قوى فاندرفال فمثلاً تكون درجات غليان متشكلات الصيغة الجزيئية C5H12 هي :-
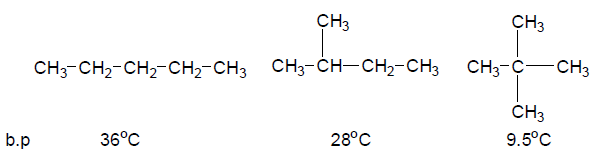
(ب) تزداد درجة الغليان بزيادة تماثل جزئ المركب بسبب انتظام شكل جزيئاته ، مثال : الصيغة الجزيئية C6H14
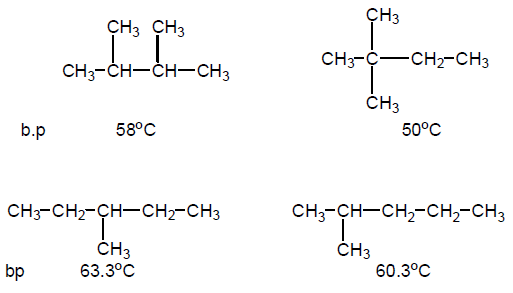
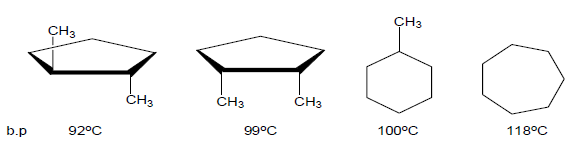
(جـ) درجة غليان الألكانات الحلقية أعلى من درجة غليان الألكانات غير الحلقية
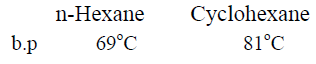
(د) تقل درجة غليان الألكانات الحلقية بوجود مجموعات ألكيل مستبدلة .
(هـ) درجة غليان المتشكل الهندسي Cis أعلي من درجة غليان المتشكل Trans ، مثال : الصيغة الجزيئية C7H14
ثانياً/ درجة الغليان للألكينات Boiling point of alkenes
- تزداد درجة الغليان بزيادة الوزن الجزيئي وتقل بزيادة التفرع.
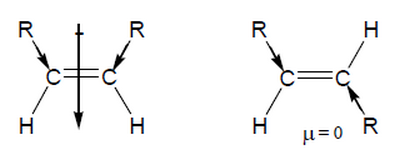
- فى الألكينات التى يوجد بها تشكل هندسي نجد أن متشكل Cis له درجة غليان أعلى من متشكل trans وذلك بسبب العزم القطبي الذي يزيد من قطبية الجزئ.
- الجدول التالي يقارن بين درجات غليان الألكانات والألكينات والدايينات المقابلة:
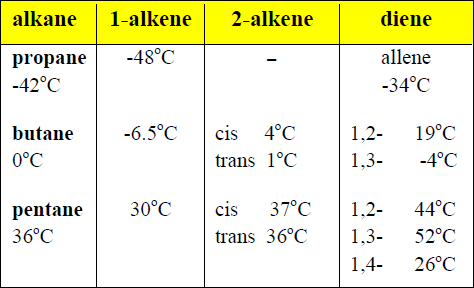
- درجة غليان الألكينات الوسطية أعلى من درجة غليان الألكانات المقابلة وذلك بسبب القطبية الناتجة عن الرابطة الزوجية.
- الجدول التالي يوضح درجات الغليان والانصهار لبعض الإلكينات:
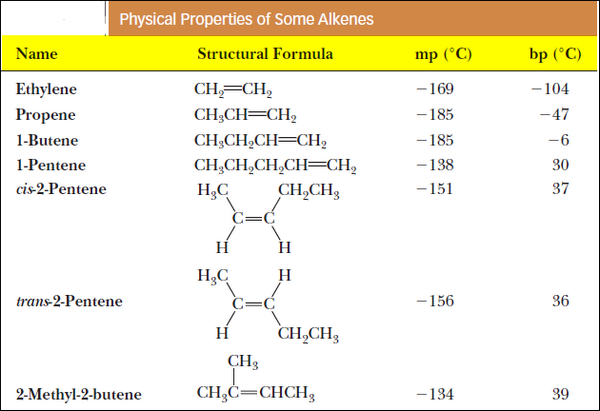
السؤال: هل الألكانات أم الألكينات أعلى في درجة الغليان؟
- الألكينات، مثل الألكانات، مواد غير قطبية، لذا فإن ذائبيتها قليلة في الماء، وتكون درجات انصهارها وغليانها منخفضة.
- لكن الألكينات أكثر نشاطا من الألكانات؛ حيث الرابطة المشتركة الثانية تزيد من الكثافة الإلكترونية بين ذرتي الكربون، مهيئة بذلك موقعاً جيداً للنشاط الكيميائي. وهذا يجعل المواد المتفاعلة قادرة على جذب إلكترونات الرابطة باي بعيدا عن الرابطة الثنائية.
- تزداد درجة الغليان بزيادة الوزن الجزيئي للمركب وذلك لأن قوى فاندرفال بين الجزيئات تزداد.
- فى أبسط الأشكال (أى لا توجد أى استبدالات على المركب) تكون الألكانات والألكينات التى لهما نفس العدد من ذرات الكربون متشابهة قليلاً فى درجات الغليان أو تكون الألكانات أعلى بقليل فى درجة الغليان لأنها أعلى فى الوزن الجزيئي. وهذا ما يحدث فى العمود الأول والثاني فى الجدول التالي.
Alkane > 1-alkene
- لاحظ الجدول التالير يوضح الفرق بين درجات غليان الألكانات والألكينات والدايينات المقابلة:

- درجة غليان الألكينات الوسطية أعلى من درجة غليان الألكانات المقابلة (التى لها نفس عدد ذرات الكربون) وذلك بسبب القطبية الناتجة عن الرابطة الزوجية. وهذا ما يحدث فى العمود الأول والثالث من الجدول السابق.
Alkane < 2-alkene
- الخلاصة هنا هو اختلاف موضع الرابطة الثنائية على الألكينات هو الذي يؤثر على درجة الغليان وذلك لزيادة القطبية الناتجة على الرابطة المزدوجة.