طبيعة المواد الداخلة في التفاعل
نقصد بطبيعة المواد المتفاعلة هو اختلاف الخواص الفيزيائية والكيميائية للمواد المتفاعلة ، فمثلاً :
(1) اختلاف عدد ونوع الروابط بين الذرات الموجودة في المواد المتفاعلة
(2) اختلاف عدد ونوع الذرات المكونة للمواد المتفاعلة .
(3) اختلاف حـالة المواد المتفاعلة من حيث كونها صلبة او سائلة أو غازية ، بالإضافة إلى كونها مشحونة او غير مشحونة .
ولتوضيح ذلك سوف نأخذ التطبيقات التالية :
تطبيقات عملية لتوضيح اعتماد سرعة التفاعل على طبية المواد المتفاعلة
تطبيق رقم (1) :اختلاف الخواص الكيميائية للمواد المتفاعلة.
أيونات الحديد ++Fe تتفاعل مع البرمنجنات -MnO4 بشكل أسرع من تفاعل الأكسالات --C2O4 مع البرمنجنات -MnO4 حسب المعادلات التالية:
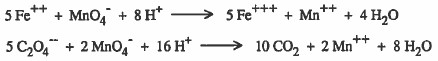
وسبب ذلك اختلاف طبيعة أيونات الحديد عن أيونات الأوكسالات حيث يتطلب في الأوكسالات --C2O4 كسر روابط تساهمية .
- اختلاف الخواص الكيميائية للمواد المتفاعلة يؤثر على سرعة التفاعل.
تطبيق رقم (2): النشاط الكيميائي للمواد المتفاعلة
- الصوديوم يتفاعل مع الماء بشكل أقوى واسرع من المغنيسيوم:
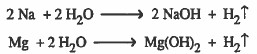
- وسبب ذلك اختلاف طبيعة الصوديوم عن المغنيسيوم حيث أن الصوديوم أكثر نشاطاً من المغنيسيوم.
تطبيق رقم (3): الحالة الفيزيائية للمواد المتفاعلة
- بعض المواد لا تتفاعل عندما تكون في الحالة الصلبة ، ولكن عندما تكون على شكل محلول فإنها تتفاعل.
- فمثلاً عند وضع كبريتات البوتاسيوم الصلب K2SO4 مع نترات الباريوم الصلبة (BaNO3) فإنهما لا يتفاعلان ، ولكن إذا خلطنا المادتين وهما على شكل محاليل فإنهما يتفاعلان كما يلي:

تطبيق رقم (4): مساحة السطح المعرض للتفاعل
تعتمد سرعة التفاعل على مساحة منطقة التلامس للمواد المتفاعلة فمثلاً برادة الحـديـد تـتـفـاعل مع الأكسجين (تصـدا) بشكل اسرع من تفاعل قضيب الحديد إذا تساوت كتلتيهما (علل) لأن مساحة منطقة التلامس لبرادة الحديد المعرضة للأكسجين أكبر من قضيب الحديد
- تحترق قطع الخشب الصغيرة أسرع من احتراق قطع الخشب الكبيرة والسبب أن اختلاف طبيعة الخشب الصغير عن الخشب الكبير حيث ان مساحة سطح التماس للخشب الصغير المعرضة للأكسجين أكبر منها للخشب الكبير.
قواعد هامة متعلقة بطبيعة المواد المتفاعلة وتأثيرها على سرعة التفاعل
(1) تفاعل الأيونات أسرع من الذرات وتفاعل الذرات أسرع من الجزيئات .
(2) تفاعل الجزيئات قليلة الروابط أسرع من الجزيئات كثيرة الروابط .
(3) تفاعل الايونات قليلة الروابط اسرع من الأيونات كثيرة الروابط .
أسئلة محلولة للتوضيح
سؤال(1): أي التفاعلين أسرع .
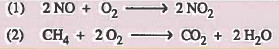
جواب : التفاعل الثاني .
سؤال(2): أي التفاعلين أسرع .
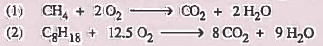
جواب : التفاعل الثاني .
سؤال(3): قارن بين سرعة التفاعلات التالية:
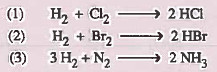
جـوا :
- التـفـاعل الثالث هو الأبطا ، وذلك لأن النـيـتـروجين يـحـتـوي على رابطة ثلاثية .
- والتفاعل الأول أبطأ من التـفـاعل الثاني ، وذلك لأن طول الرابطة في Br2 أطول (أضعف) منها في Cl2 وذلك بسبب أن الحجم الذري للبروم أكبر من الكلور.
سؤال(4): أي التفاعلات التالية ينتج غاز الهيدروجين بشكل أسرع:
(أ) قطعة خارصين مع حمض الكلور (0.2M).
(ب) مسحوق الخارصين مع حمض الكلور (0.2M).
جواب: مسحوق الخارصين أسرع ، وذلك لزيادة مساحة منطقة التلامس المعرضة لحمض الكلور.
سؤال(5): أيهما أسرع تفاعلاً:
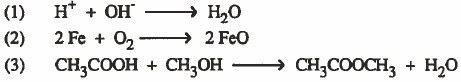
الحل: التفاعل الأول أسرع