المواد الحافزة
- تعريف المواد الحافزة هي مواد تزيد من سرعة التفاعل دون أن تستهلك.
- ونقصد بعبارة (دون أن تستهلك) أي دون أن يحدث للمادة الحافزة أي تغير كيميائي في تركيبها بعد انتهاء التفاعل ، وهذا يدل على انه يمكن استعادة المادة الحافزة بعد انتهاء التفاعل واستخدامها مرة أخرى.
- مثال عند حدوث تفاعل بين المادة A مع المادة B في وجود العامل الحافز D فإن التفاعل يتم كما يلي:
A +D → AD
AD + B → AB + D
لاحظ أن المادة الحافزة D دخلت في التفاعل وخرجت من التفاعل دون أن تستهلك.
أمثلة على المواد الحافزة
(1) أكاسيد الحديد تزيد من سرعة تفاعل النيتروجين مع الهيدروجين لإنتاج النشادر.
2H2 + N2 → 2NH3
(2) انزيم الببسين يزيد من سرعة هضم البروتينات في المعدة.
(3) ثاني أكسيد المنجنيز MnO2 يزيد من سرعة تفكك فوق أكسيد الهيدروجين H2O2 الماء وغاز الأكسجين :
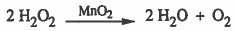
(4) أيونات المنجنيز (--Mn) تزيد من سـرعـة تفاعل البرمنجنات ( -MnO4) مع الأوكسالات (--C2O4)
أمثلة محلولة للتوضيح
مثال (1): التفاعل التالي:
O3 + O → 2O2
يمر في خطوتين:
O3 + NO → NO2 + O2
NO2 + O → NO + O2
حدد المادة الحافزة .
الحل:
المادة الحافزة هي المادة (NO)لأنها دخلت في التفاعل وخرجت منه دون أن تستهلك (يتغير تركيبها الكيميائي).
مثال (2): التفاعل التالي :
2SO2 + O2 → 2SO3
لا يتم إلا في وجود مادة حافزة كما يلي:
2NO + O2 → 2NO2
2NO2 + 2SO2 → 2SO3 + 2NO
حدد المادة الحافزة .
الحل:
المادة الحافزة هي المادة (NO) لأنها دخلت في التفاعل وخرجت منه دون ان تستهلك (يتغير تركيبها الكيميائي).
أنواع عمليات الحفز
(1) الحفز المتجانس ( homogeneous catalysis ):
هو الذي يكون فـيـه الـحـفـاز مـن نفس حالة المواد المتفاعلة
مثال:
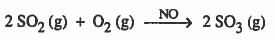
(2) الحـفـز غـيـر المـتـجـانس (Heterogeneous catalysis):
هو الذي يكون فـيـه الـحـفـاز والمواد المتفاعلة من حالتين فيزيائيتين مختلفتين
مثال:
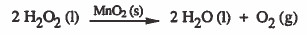
- تعريف السموم: هي تعيق عمل المواد الحافزة .
- مثال على السموم : الكبريت يقلل من فـعـالـيـة أكـاسـيـد الحـديـد كـمـادة حـافـزة تساعد على زيادة سرعة تفاعل النيتروجين مع الهيدروجين لإنتاج النشادر .
العوامل المؤثرة على سرعـة الـتـفـاعـل
يتبين من دراسة أثر العوامل المؤثرة على سرعـة الـتـفـاعـل أن هناك أمـور تزيد مـن سـرعـة التفاعل وهي:
- نقص عدد الروابط زياد
- تركيز المحاليل
- زيادة النشاط الكيميائي
- زيادة درجة الحرارة .
وضع مادة حافزة مناسبة
- زيادة الضغط على التفاعلات الغازية
- زيادة مساحة سطح التماس