الخواص الفيزيائية للكحولات
- تتميز الرابطة بين الأكسجين والهيدروجين فى مجموعة الهيدروكسيل بالقطبية O-δ - H+δ
- وتنعكس قطبية هذه الرابطة على الخواص الفيزيائية لأفراد طائفة الكحولات.
- فعندما نقارن درجات غليان الكحولات مع درجات غليان الهيدروكربونات المقاربة لها تقريباً ، في الأوزان الجزيئية، نجد أن الكحولات تغلي عند درجات أعلى بكثير.
- على سبيل المثال يغلي ١ - بروبانول (وزنه الجزيئي: ٦٠) عند درجة ٩٧مo ، بينما نجد أن البيوتان النظامي (وزنه الجزيئي: ٥٨) يغلي عند درجة الصفر المئوى.
- لجزيئات الكحولات القدرة على انشاء روابط هيدروجينية مع بعضها البعض إذ تتجمع وفقاً للآتي:
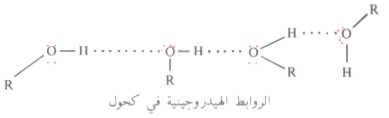
وهذا الترابط الهيدروجيني هو السبب المباشر في ارتفاع درجات غليان الكحولات.
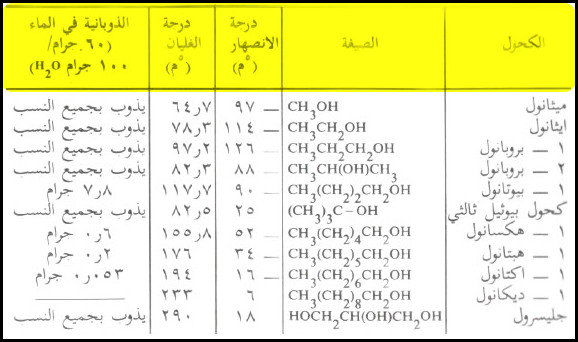
- تذوب الكحولات البسيطة فى الماء بأي نسبة (حسب الجدول).
- وابتداء من الفرد الرابع غير المتفرع فإن الذوبانية في الماء تقل تدريجياً بازدياد عدد ذرات الكربون في جزيء الكحول.
- فالكحولات ذات السلسلة الهيدروكربونية الطويلة نجد أنها أكثر شبهاً بالهيدروكربونات.
- ويبين الجدول التالي الخواص الفيزيائية لبعض الكحولات: