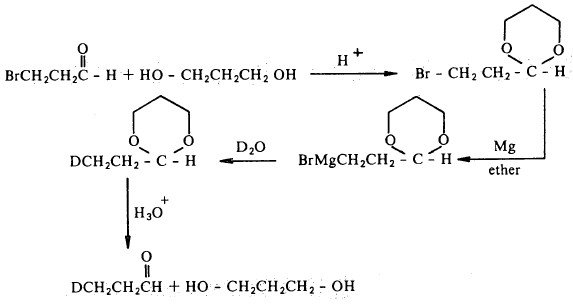
تكوين الأسيتال والكيتال من الألدهيدات والكيتونات
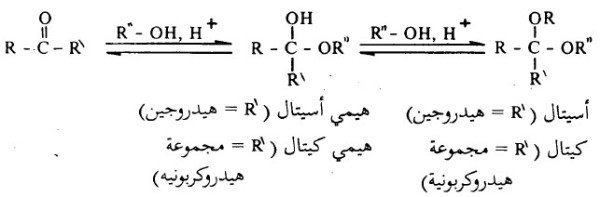
- تضاف الكحولات إلى الألدهيدات، بطريقة مشابهة لتفاعلها مع الماء تحت ظروف حمضية أو قاعدية وتختلف النواتج باختلاف الوسط.
أولاً/ إضافة الكحولات إلى الأدهيدات والكيتونات فى الوسط الحمضي
- يتكون ما يعرف بالهيمي أسيتال إذا ما تم إضافة الألدهيد إلى جزىء من الكحول.
- ويتكون ما يعرف بالأسيتال من إضافة الزيادة من الكحول إلى الهيمي أسيتال.
- هذا ويعرف ناتج الإضافة بالهيمي كيتال أو الكيتال من إضافة جزيء أو جزيئين من الكحول إلى الكيتون على التوالي.
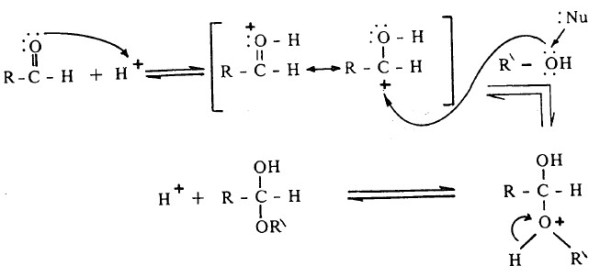
- يتكون أيون الأكسونيوم عند إضافة بروتون إلى ذرة أكسجين مجموعة الكربونيل، ومن ثم يتم الهجوم النيكلوفيلي على ذرة كربون الأكسونيوم، وفي الخطوة الأخيرة يتكون الهيمي أسيتال كما يتضح من التالي:
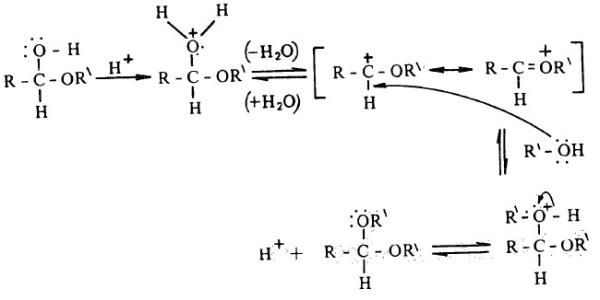
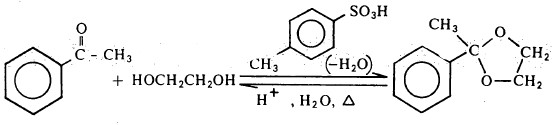
- كما أشرنا سابقاً، فإن الاسيتال يمكن أن يتكون من تفاعل الكحول مع الزيادة من الألدهيد في وجود الحفز الحمضي - غالباً ما يكون غاز كلوريد الهيدروجين وكبريتات الماغنسيوم الجافة - لنزع الماء من وسط التفاعل أولاً بأول.
- وميكانيكية تكون الأسيتال تشتمل على إزاحة الماء من الهيمي أسيتال المحفزة بالحامض يليها إضافة الكحول.
- هذا ويمكن أن تتم إزاحة الماء من وسط التفاعل في مثل هذه التفاعلات بتصميم جهاز التفاعل بطريقة تسمح بإزاحة الماء بواسطة التقطير الأزوتروبي.
- وزيادة الكحول وإزاحة الماء في هذا التفاعل تجعل الفرصة مواتية بصورة أكبر لسير التفاعل باتجاه اليمين (أي جهة تكوين الأسيتال).
- وعلى العكس فإن إذابة الأسيتال في الماء وإضافة قليل من الحامض يجعل الاتزان يميل جهة اليسار أي نحو تكوين الألدهيد (يتميأ الأسيتال).
- وميكانيكية هذا التحلل المائي للأسيتال هو الطريق العكسي تماماً لميكانيكية تكونه.
- وفي الغالب يتكون الأسيتال من الكحولات البسيطة مع الألدهيدات، في حين أن الكيتال نادراً ما يتكون من هذه الكحولات (قد يتكون بمردود ضعيف جداً) ولكن يتكون من تفاعل الجليكولات (الكحولات ثنائية مجموعة الهيدروكسيل) مع الكيتونات.
ومما تجدر الإشارة إليه أن معظم السكريات توجد بصورة رئيسية على هيئة هيمي أسيتال أو هيمي كيتال حيث أن جزىء السكر يحوي مجاميع هيدروكسيل عديدة ومجموعة كربونيل في نفس الجزىء.
ثانياً/ إضافة الكحولات إلى الألدهيدات والكيتونات فى الوسط القاعدي
- يمكن أن يتكون الهيمي أسيتال أو الهيمي كيتال في الوسط القاعدي.
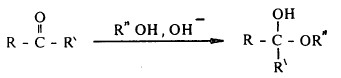
- وميكانيكة هذا التفاعل مشابهة تماماً للإضافة النيكلوفيلية لسيانيد الهيدروجين إلى مركبات الكربونيل.
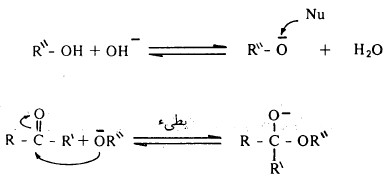
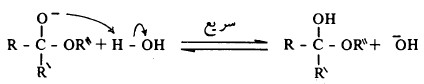
- على الرغم من أن الأسيتالات والكبتالات تتمياً إلى الدهيدات وكيتونات في الأوساط الحامضية المائية إلا أنها ثابتة في الأوساط القاعدية المائية.
- وبسبب هذه الخاصية الأخيرة فإن الاسيتالات والكيتالات تقدم وسيلة جيدة لحماية مجموعة كربونيل الألدهيدات والكيتونات من تفاعلات لا نرغب في حدوثها فيحول الألدهيد أو الكيتون إلى أسيتال أو كيتال ويجرى عندئذ التفاعل وأخيراً يمكن تميؤ الأسيتال أو الكيتال لاستعادة مجموعة الكربونيل.