ملاحظات حول كيفية تحضير الدفتر العملي في معمل الكيمياء
(1) يقوم الطالب خلال العمل المخبري بكتابة تجارية في دفتر عملي خاص به وموحد - ويبدأ تسجيل الجلسة بكتابة تاريخها ورقمها، يلى ذلك عنوان كل تجربة يقوم بها الطالب مع شرح مبسط لها وفقاً للملاحظات الواردة أدناه.
(2) يجب أن يسجل الطالب عمله المخبري تسجيلاً مرتباً مباشرة بعد إنجاز كل تجربة مبيناً الملاحظات التي أثارت انتباهه خلال العمل (كتغير اللون - وتشكل الراسب أو انحلاله - وظهور روائح مميزة ... الخ)
(3) لا يجوز أبدأ تأجيل كتابة الملخص العملي إلى البيت ثم كتابته بعد ذلك من الذاكرة .
(4) لا يجوز مطلقاً نسخ التجارب كما هو وارد في الكتاب
(5) يجب التعبير قدر الامكان بوساطة الصيغ مع الاستعانة بكتابة الأسهم وذكر شروط التفاعل والملاحظات ... إلخ.
- إن الاستعمال البارع للتعبير بالصيغ يساعد على اختصار الوقت.
- ولنأخذ مثلاً على هذا ، هذه الجملة الطويلة ( إذا أخذنا مادة عضوية ما حاوية الآزوت وصهرناها مع الصوديوم المعدني فإن الصوديوم ينتزع من المادة ذرة الآزوت مع ذرة الكربون ويكون سيانيد الصوديوم ). ويمكن التعبير عن هذه الجملة بسطر واحد هو
CN + Na → NaCN.....
(6) لا يجوز الاعتماد على التعبير بالصيغ إذا كان هناك ملاحظة هامة يجب ذكرها وفي هذه الحالة يجب أن تكون الكتابة واضحة ومحددة ومختصرة.
(7) لا يجوز للمبتدئين في دراسة الكيمياء العضوية أن يبدأوا دراستهم باستعمال صيغ المركبات العضوية والجملة البسيطة وغير النظامية التي قد تبدو لهم للوهلة الأولى أسهل من الصيغ المفصلة والمنشورة.
مثال: إن حفظ الصيغ المجلة:
CH3 COOC2 H5 | CH3 COC2H5 | CH3 CHO
- يجعل من الصعب على الطالب معرفة مع أي ذرة تتصل ذرة الأكسجين في الصيغة الأولى ومع أي ذرة يرتبط جذر الأثيل في الصيغتين الثانية والثالثة.
(8) إن الوقت الضائع في البداية لا يذهب سدى إذ بفضله يكتسب الطالب خبرات جيدة في فهم الصيغ البنيوية.
- وهذه الخبرات ضرورية ولا سيما عند دراسة المركبات العضوية المعقدة كالسكريات والتربينات والدهون والحلقات غير المتجانسة
(9) ستدل التجارب على أن الغالبية العظمى من التفاعلات تنتمي إلى عدد محدود من العمليات الكيميائية كانفصام الماء أو انضمامه ، واختزال المواد أو أكسدتها ، وتفاعلات الانضمام المختلفة عند مكان انضمام الرابطة الثنائية... إلخ.
ولهذا فعند دراسة هذه التفاعلات يجب التنبه أولاً إلى نوع التفاعل الجاري وليس إلى النواتج النهائية للتفاعل التى يمكن أن تكون متنوعة ومختلفة.
مثال: عند تفاعل الكحولات المختلفة مع الأحماض يمكن الحصول على عشرات أو مئات الاسترات. إلا أنه في جميع الحالات يلاحظ دوماً انفصال جزئيات الماء الذي يعد الحلقة الرئيسة في التفاعل المدروس . ولهذا فعند كتابة المعادلات يجب ترتيب الصيغ حيث يصبح من السهل الإشارة إلى العملية الرئيسة في التفاعل وهي في مثالنا انفصال الماء المشار إليه بالخطوط المنقطة واتحاد بقيتي الحمض والكحول:
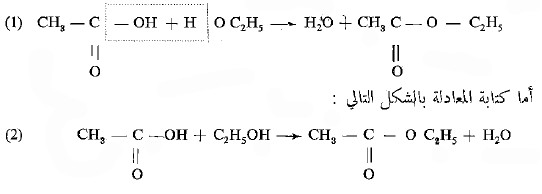
فيجعل توضيح عملية انفصال الماء صعباً .
- إن تمثيل المعادلة بالشكل (1) يجعل تعميم المعاداة على جميع الاسترات سهلاً
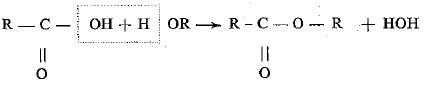
(10) لايجوز استعمال الصيغ المنشورة إلا إذا كانت هناك حاجة إلى ذلك . فمثلاً يجب استعمال الصيغة المنشورة للكحول الاثيلي عند دراسة آلية استحضار الكحول الاثيلي أو استحضار أسيتألدهيد أي في التفاعلات التي يحصل فيها تغير في بنية جذر الأثيل .
- أما إذا كان التفاعل لا يتضمن تغيراً في بنية جذر الاتيل كما في استحضار كلوريد الأثيل أو الاثير الاثيلي من الكحول الاتيلي فعندئذ ليست كتابة الصيغة المنشورة للكحول الاثيلي ضرورية.
(11) على الطالب أن يتعود منذ البداية كتابة الصيغ كتابة دقيقة ويجب عليه أن يراعي أيضاً صحة كتابة الروابط بين الذرات المختلفة أو الرموز الوظيفية لأن كتابة الصيغ بشكلها الصحيح يسهل ملاحظة تكافؤات الذرات ملاحظة واضحة.
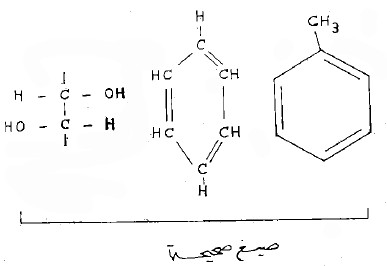
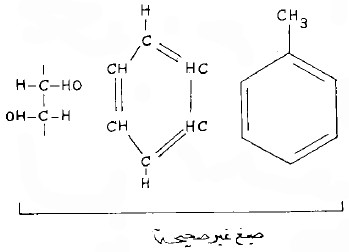
(12) إذا ارتبطت الزمر الوظيفية COOH - SOH, HO - بالجانب الأيسر من السلاسل الكربونية أو الحلقات فيجب كتابتها بشكل معاكس وذلك لإظهار ذرات السلسلة أو الحلقة التي ترتبط بها هذه الزمر.