تحضير الميثان من خلات الصوديوم (اسيتات الصوديوم)
خطوات التجربة
- ضع في أنبوب اختبار مجهز بسدادة تخترقها أنبوبة توصيل كما بالشكل التالي وعلى ارتفاع 10 مم مزيجاً من كميتين متساويتين وزناً من خلات الصوديوم والكلس الحي اللامائيتين بعد تكليسهما.
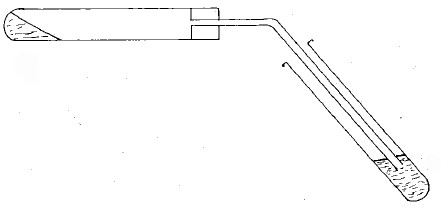
- اجعل الأنبوب في وضع أفقي وسخنه على لهب واحرق غاز الميثان المنطلق من فتحة الأنبوب (في البداية يمكن إبعاد أنبوب توصيل الغاز) ولاحظ اشتعال الميثان بلهب غير مضيء .
- غير أن الميثان يشتعل أحياناً بلهب أصفر بسبب وجود الصوديوم في الزجاج (يجب ألا يخلط بين اصطلاح (غير مضيء) و اصطلاح (غير ملون) إذ إن اللهب يمكن أن يكون غير مضيء ولكنه يكون في الوقت نفسه ملوناً باللون الأزرق أو اللون الأصفر).
- بعد التأكد من أن الميثان يشتعل، اغمس أنبوب خروج الغاز في أنبوب اختبار حاو كمية قليلة من محلول برمنجنات البوتاسيوم والمحضرة بإضافة قطرة من محلول 0.1N برمنجنات البوتاسيوم إلى 5 قطرات من الماء.
- وتأكد من أنه لا يحصل زوال للون محلول البرمنجنات عند إمرار الميثان فيه لأن الميثان في هذه الشروط لا يتأكسد .
- وبعد ذلك اغمس نهاية أنبوب توصيل الغاز في أنبوب اختبار ثالث حاو 5 قطرات من ماء البروم .
- تأكد من عدم زوال لون ماء البروم ، وفي هذه الشروط أيضاً لا يتفاعل الميثان مع البروم وذلك لأن الميثانن هيدروكربون مشبع.
- وبصورة مشابهة للميثان فإن الهيدروكربونات الأخرى لا تتفاعل مع برمنجنات البوتاسيوم أو ماء البروم ولذلك فهي تسمى بالبارافينات وتسميتها مستمدة من الكلمتين اللاتينيتين (Parum, affinis) أي القليلة الألفة.
نظرية التجربة
- من التجربة المدروسة نستطيع تأكد من أنه عند تسخين خلات الصوديوم مع الصود الكاوي يتكوّن غاز الميثان.
- عملياً يستبدل الكلس الصودي وهو مزيج من ماءات الصوديوم والكلس الحي وذلك لأن الزجاج يتأكل بفعل الصود الكاوي عند التسخين.
- يتكون بالإضافة إلى غاز الميثان كربونات الصوديوم التي يمكن الكشف عنها بعد أن يبرد الأنبوبة (الأنبوبة اليمنى فى الشكل السابق) بإضافة 2-3 قطرة من محلول (HCl) تركيز 2N فتنطلق فقاعات غاز CO2.
- يمكن التأكد من انطلاق CO2 بإغلاق الأنبوب بالسدادة المجهزة بأنبوب توصيل الغاز ثم إمرار الغاز المنطلق في أنبوب حاو 3 قطرات من محلول هيدروكسيد الباريوم المشبعة 2(Ba(OH الشفافة.
- لاحظ تعكر محلول هيدروكسيد الباريوم نتيجة لتشكل راسب من BaCO3
Na2CO3 + 2HCl → 2NaCl + H2CO3
↑ H2CO3 ↔ H2O + CO2
H2CO3 + Ba(OH)2 → BaCO3↓ + 2H2O
معادلة تحضير الميثان
- فيما يلي معادلة تحضيرالميثان:
CH3COONa + NaOH → CH4 + Na2CO3