الخواص الكيميائية لعناصر الفلزات القلوية
- فلزات المجموعة 1A هي من أكثر الفلزات المعروفة نشاطاً وفاعلية (ما عدا الهيدروجين).
- بسبب نشاطها ، لا توجد تلك الفلزات منفردة في الطبيعة، لكنها توجد متّحدة مع اللافلزات كأملاح قلوية.
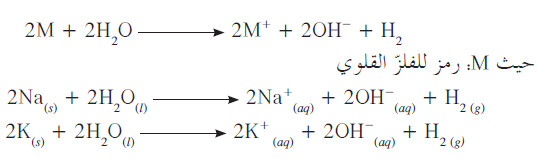
(أ) التفاعل مع الماء
- يتفاعل كل فلز من الفلزات القلوية بشدة مع الماء البارد منتجاً غاز الهيدروجين ومحلولًا من هيدروكسيد الفلز القلوي (يُعرف ببساطة بمحلول قاعدي أو قلوي).
- على سبيل المثال ، يتفاعل الصوديوم مع الماء البارد بعنف مكوّناً هيدروكسيد الصوديوم ومطلقاً غاز الهيدروجين.

- تتفاعل الفلزات القلوية سريعًا مع الماء.
- هذا التفاعل طارد للحرارة لدرجة أنه غالبًا ما يشتعل الهيدروجين بمجرد تكوينه.
- تتفاعل الفلزات القلوية أيضًا بقوّة مع الرطوبة الموجودة في جلد الإنسان ، لذلك يجب عدم لمسها مباشرة باليد بدون ارتداء قفازات واقية.
- يتم تخزين الفلزات القلوية دائما تحت سطح الزيت أو الكيروسين لحفظها من التفاعل مع بعض مكونات الهواء الجوي.
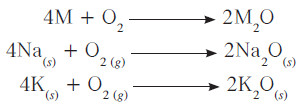
(ب) التفاعل مع الأكسجين
- تتفاعل الفلزات القلوية مع أكسجين الهواء لتنتج مركبات صلبة تبعاً للمعادلة التالية:
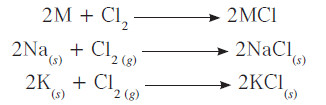
(جـ) التفاعل مع الهالوجينات
- تتفاعل الفلزات القلوية مباشرة مع الهالوجينات مثل غاز الكلور تبعًا للمعادلة التالية: