لأنه أكثر الأشكال استقراراً بسبب تباعد ذرات الهيدروجين كأكثر ما يكون التباعد عندما تكون الزوايا بينها وبين بعضها مروراً بذرة الكربون المركزية 109.28 وذلك بسبب عملية التهجين
تعريف التهجين Hybridization
- يعطى التهجين تفسيراً لطبيعة الأفلاك الذرية وكيفية اتحادها لتكوين الأفلاك الجزيئية وهى عبارة عن عملية تداخل بين أفلاك الذرة الواحدة المتقاربة في الطاقة ينتج عنها افلاك جديدة متساوية في الطاقة والشكل.
تهجين وبناء جزئ الميثان CH4 - Methane
H1: 1s1 , 6C: 1s2, 2s2 2p2
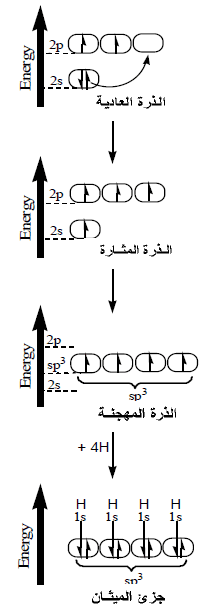
(1) من التوزيع الإلكتروني لذرة الكربون نجد أنها تحتوى على مزدوج إلكتروني في الفلك الفرعي (2s) وإلكترونين مفردين في الفلك الفرعي (2p).
(2) عند إثارة الذرة ينتقل إلكترون من الفلك الفرعي (2s) إلى الفلك الفرعي (2p) فتمتلك بذلك ذرة الكربون 4 افلاك نصف ممتلئة ولكنها غير متماثلة في الشكل والطاقة.
(3) يحدث تهجين بين أفلاك (2s) وأفلاك (2p) في مستوى طاقة اعلى من مستوى طاقة الفلك (2s) وأقل من مستوى طاقة الفلك (2p) فتتكون 4 أفلاك متماثلة في الشكل والطاقة.
(4) تسمى الأفلاك المهجنة بأفلاك (sp3) لأنها نتجت من تهجين فلك (s) مع ثلاثة أفلاك (p)
(5) تتنافر الأفلاك المهجنة فيما بينها حتى تصل زوايا الربط (Bond angle) إلى 109.5o
(6) يتم التداخل بين الأفلاك المهجنة وفلك (1S) لأربع ذرات هيدروجين فتتكون 4 روابط تساهمية أحادية من النوع سيجما (Sigma bond) وبذلك يتكون جزئ الميثان.
(7) عدد الروابط المتكونة في جزي الميثان أربعة روابط كلها من النوع سيجما.
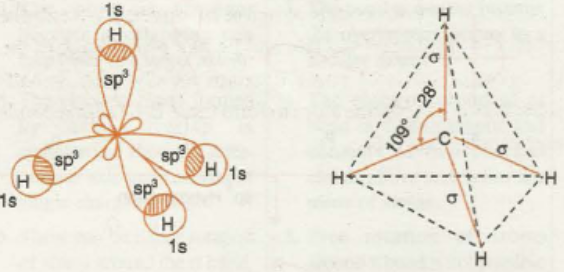
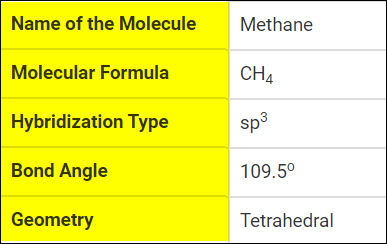
(8) من خلال دراسة تهجين جزئ الميثان نستنتج أن الشكل الهندسي له هو هرم رباعي الأوجه Tetrahedral
ملاحظات هامة
(أ) الرابطة سيجما : (σ) (Sigma bond) هي رابطة تنشأ من التداخل الأفقي للأفلاك أي تكونت على خط واحد.
(ب) لا ترتبط ذرات الهيدروجين مع ذرة الكربون المثارة لأن الأفلاك تكون متعامدة بزوايا 90o وكذلك وجود نوعين من الأفلاك المختلفة في الشكل والطاقة (s, p).