قاعدة هوند Hund's law
- تنص قاعدة هوند على أن :
" لا يحدث ازدواج بين إلكترونين في مستوى فرعي معين إلا بعد أن تشغل أوربيتالاته فرادي أولاً"
- إن حقيقة تنافر الإلكترونات المشحونة بشحنة سالبة لها تأثير كبير في توزيع الإلكترونات في مستوىات فرعية متساوية الطاقة.
- وتنص قاعدة هوند على أن الألكترونات تتوزع في المستوىات الفرعية المتساوية الطاقة بحيث تحافظ على أن يكون لها الاتجاه نفسه من حيث الدوران، قبل ان تشغل الإلكترونات الإضافية ذات اتجاه الدوران المعاكس المستويات نفسها.
- على سبيل المثال: تُملأ مستويات (2p) الفرعية الثلاثة بإلكترونات منفردة ، ثم يحدث الأزدواج.
- يوضح الشكل التالي طريقة تسلسل دخول ستة إلكترونات في مستويات (p) الفرعية:
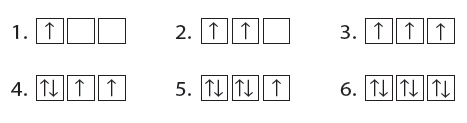
مثال (1): كتابة التوزيع الألكتروني لذرة النتيروجين N7
يكون التوزيع الألكترونى كالتالي:
N7 : 1S2 , 2S2 , 2p3

شرح التوزيع:
- عند التوزيع الألكتروني لذرة النيتروجين نجد ان المستوى الفرعي (2p) يحتوى على ثلاث إلكترونات.
- وكما نعلم أن المستوى الفرعي (2p) يحتوى على ثلاث أوربتالات px , py , pz وهى متساوية فى الطاقة. فكيف تتوزع الألكترونات الثلاثة بين الأوروبتالات الثلاثة؟
- تبعاً لقاعدة هوند نجد أن كل ألكترون يشغل أوربتالاً مستقلاً لأن ذلك أفضل له من جهة الطاقة. لأنه عند ازدواج إلكترونين في أوربتال واحد وبالرغم من أن غزلهما معاكس إلا أن هناك قوى تنافر بينهما تعمل على تقليل استقرار الذرة (زيادة طاقتها).
يلاحظ أن الحركة المغزلية المفردة تكون فى اتجاه واحد وهذا الوضع يعطي الذرة أكبر قدر من الاستقرار.
مثال (2): كتابة التوزيع الألكتروني لذرة النتيروجين O8
- يكون التوزيع الألكتروني كالتالي:
O8 : 1S2 , 2S2 , 2p4
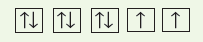
شرح التوزيع:
- نجد أن المستوى الفرعي (2p) به أربعة إلكترونات تتوزع ثلاثة منها أولاُ على الثلاثة أوربتالات (2p) وذلك حسب قاعدة هوند.
- أما الألكترون الرابع فأمامه احتمالين:
الأحتمال الأول: أن يدخل أحد الأوربتالات الثلاثة السابقة ويزدوج مع أى إلكترون موجود فيها وهناك سيعاني من التنافر مع الألكترون الموجود أصلاً.
الأحتمال الثاني: أن يصعد إلى المستاوى الفرعي التالي وهو (3s) ذو الطاقة الأعلى من (2p).
إلا أنه لا يزال الأفضل من جهة الطاقة لأى إلكترونين لهما غزل متضاد أن يزدوجا في نفس الأوربتال عن أن ينتقل أحدهما إلى المستوى الفرعي التالي الأعلى فى الطاقة.